Ligações Ácido carbônico.
Porque o ácido carbônico (H2CO3), possui uma ligação dupla e duas simples? Porque não H4CO4, fazendo quatro ligações simples?
💡 2 Respostas
Vinícius Galiza
Uma resposta está na estrutura dessas moléculas, sobretudo, a estabilidade que elas apresentam. O H2CO3 é um ácido instável e, facilmente se decompõe em CO2 e H2O, mas ele deve apresentar maior estabilidade que H4CO4. Sabendo que o oxigênio tem elevada eletronegatividade, a proximidade de grupos pequenos contendo esse átomo, como o OH, causa instabilidade na espécie química. Analisando a geometria: H2CO3 é trigonal planar, com grupos O, OH, OH separados de ângulos de 120 graus; H4CO4 é tetraédrico, com grupos OH separados de ângulos de 109,5 graus (aproximadamente), ou seja, no H4CO4 os grupos oxigenados estão mais próximos, logo, essa molécula será mais instável que o H2CO3.
Especialistas PD
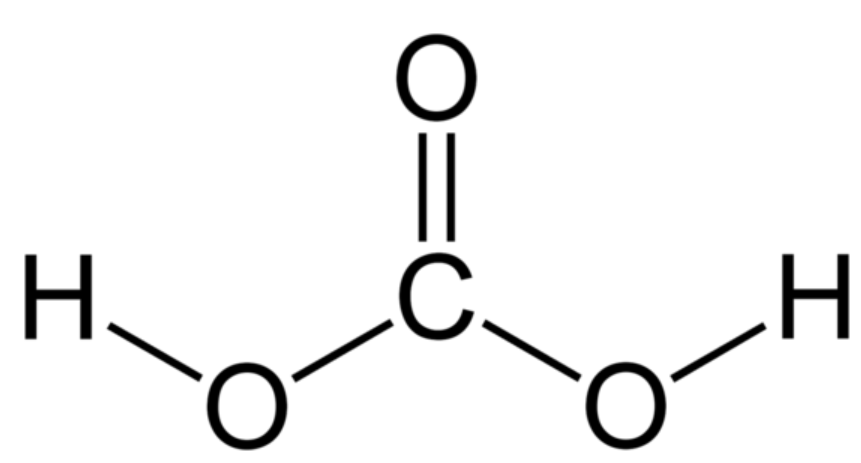
O ácido carbônico possui a fórmula H2CO3. Com o carbono, com 4 elétrons na camada de valência, compartilhando elétrons com 3 oxigênios (2 ligações simples e 1 dupla) e dos 3 oxigênios, 2 se ligam ao hidrogênio, assim todos estão com seu octeto completo.
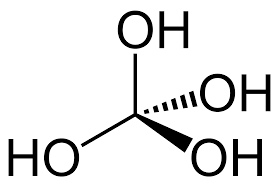
Já a fórmula H4CO4 pertence ao ácido ortocarbônico.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.







Compartilhar