Porque a água é uma molécula polar e não apresenta centro de inversão?
💡 3 Respostas
Especialistas PD
Uma molécula é polar se possuir um momento de dipolo elétrico permanente. Podemos aplicar os conceitos relacionados à simetria das moléculas, com a polaridade: uma molécula não pode ser polar se ela pertencer a um grupo que inclua um centro de inversão como elemento de simetria (mas a recíproca não é necessariamente verdadeira).
A água é polar, já que na ligação entre hidrogênio e oxigênio, os átomos de oxigênio aproximam de forma mais efetiva os elétrons, que dessa forma permanecem mais juntos dele. A partir daí, a molécula de água exibe uma região positiva, os hidrogênios, e uma negativa, o oxigênio, dando origem a uma molécula polar e/ou dipolo.
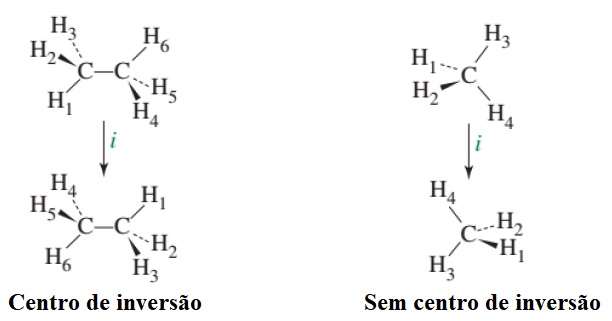
E a água não apresenta centro de inversão, esta operação de simetria projeta cada átomo da molécula em questão através de um ponto imaginário (i) e, caso a molécula resultante for indistinguível da molécula inicial esta possui cento de inversão, o que não acontece com a molécula de água. Podemos observar a diferença entre duas moléculas, uma com centro de inversão e a outra não, na figura abaixo:
Diogo Gomes
A água é uma molécula polar porque existem pólos, por causa da diferença de eletronegatividade entre os átomos. Ela não possui centro de inversão, ou centro de simetria, porque uma molécula não pode ser polar e apresentar centro de inversão.
Uma inversão envolve o movimento de cada átomo através do centro da molécula, esse elemento coincide com o centro geométrico da molécula. Qualquer ponto da molécula leva até seu centro e depois move-a com a mesma distância percorrida, no entanto, no sentido oposto da molécula.
Espero ter ajudado! =D
Luana Arruda
Mais uma vez, muito obrigada pela ajuda de sempre que me dá. Valeu ;)
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.
Perguntas relacionadas
Para determinar se uma molécula e polar ou Apolar devemos observar qual item?
Química Inorgânica I
•UNIFACVEST
Lia Francine
Materiais relacionados
 3 pág.
3 pág. 3 pág.
3 pág. 3 pág.
3 pág.




Compartilhar