Como é feita a montagem do complexo pré traducional? (Genética Molecular)
💡 1 Resposta
Junior Ogioni
Nas células eucarióticas, há uma grande quantidade de sequências de DNA que não são expressas em RNA ou em proteínas, não sendo, portanto, convertidas em produtos funcionais. Grande parte do DNA que especifica o RNA mensageiro constitui os íntrons dentro dos genes. Descobertos em 1977, por Berget, os introns são regiões dos genes que não codificam qualquer proteína, embora façam parte da transcrição inicial. Como veremos a seguir, eles separam, uma das outras, sequências de DNA que codificam para proteínas conhecidas como éxons.
Nesse caso, como mostra a figura abaixo, todo o gene, conhecido como gene em mosaico, contendo éxons e íntrons, é transcrito em uma longa molécula de RNA (pré-RNAm), dotada de éxons e íntrons. Em seguida, ocorre remoção dos íntrons, o que reduz o tamanho do RNA inicial. Finalmente, os éxons se ligam, formando o RNAm funcional ou maduro, que, contendo apenas segmentos codificadores (éxons), migra para o citoplasma, onde vai ser traduzido em cadeia polipetítidica.
Esse processamento do RNA, chamado splicing – que ocorre no núcleo e consiste na remoção dos íntrons e união éxons imediatamente após a transcrição do RNA – é bastante complexo, já que a molécula de RNA deve ser clivada em locais exatos e os éxons devem ser unidos também de maneira exata. Os íntrons retirados do pré-RNA são “destruídos” dentro do núcleo gerando nucleotídeos livres que são reciclados. A denominação íntron deriva do fato de eles, embora sejam transcritos (compõem o transcrito primário), não saem do núcleo, já que são “destruídos”, como vimos acima, neste compartimento celular.
Tanto a clivagem do pré-RNA, para remoção dos íntrons, como a junção dos éxons, para a formação do RNA funcional, envolvem um complexo enzimático chamadospliceossoma (maquinaria de splicing). O spliceossoma é constituído por 5 tipos de pequenos RNAs (dotados de 107 a 210 nucleotídeos), ricos em uracil, associados a proteínas, formando ribonucleoproteínas. Ele é um complexo dinâmico no qual os elementos que o compõem estão mudando constantemente durante o processo de amadurecimento. O splicing requer uma extrema precisão das moléculas envolvidas no processo, já que o acréscimo ou a remoção de um único nucleotídeo em um éxon pode alterar a fase de leitura e produzir uma proteína bastante diferente da original, caracterizando uma mutação, decorrente, portanto, de erros no splicing.
Em face de o splicing ser um processo complexo, com regulação fina, uma mutação em um sítio de reconhecimento da junção exon-intron ou em um elemento regulador, pode causar um erro no processo, gerando um produto aberrante, que pode, muitas vezes, inativar um gene, com graves consequências. Estima-se atualmente que erros no processo de splicing causem cerca de 10% das doenças genéticas. Por outro lado, pesquisas na área da biologia molecular poderão criar ferramentas capazes de corrigir sequências que afetam padrões de splicing, bem como expressar, inativar ou mudar a concentração de reguladores com o objetivo de reparar genes afetados por deleções, como no caso da distrofia muscular progressiva. Ressaltamos que o splicingsó ocorre em células eucarióticas, já que o DNA das células procarióticas é desprovido de íntrons.
Foi estudando o splicing de RNA ribossômico de um protozoário ciliado (Tetrahymena thermophila) que Thomas Cech descobriu, em 1982, a ribozima (RNA dotado de função enzimática), assunto que abordamos neste blog no dia 10.06.2011, sob o título “Ribozima (RNA super star)”. No ano seguinte, Sidney Altman constatou que na Rnase P, enzima que catalisa a maturação de RNAt (splicing do RNAt), a atividade enzimática é exercida pela parte ribonucleica (RNA), e não pela parte proteica da enzima.
SPLICING ALTERNATIVO/GENOMA HUMANO
As estimativas iniciais eram de que o genoma humano possuía em torno de 100 mil genes. Esse número tinha por base a quantidade de diferentes proteínas humanas, estimada em cerca de 90 mil. Deveríamos, portanto, ter pelo menos 90 mil genes para codificá-las. Os trabalhos relatando o sequenciamento de todos os cromossomos humanos (PROJETO GENOMA HUMANO) mostraram que o número de genes estruturais era bem mais baixo (da ordem de 25 mil).
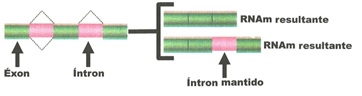
O reduzido número de genes presentes na espécie humana é hoje explicado pela sua grande versatilidade. Graças a um mecanismo chamado splicing alternativo (edição alternativa ou processamento alternativo), em que os mecanismos celulares podem, em linhas gerais, “decidir” remover um éxon ou manter um intron (figura a seguir), ou partes dele, a informação armazenada nos genes dos organismos pode ser editada de várias formas. Isto faz com que um gene possa codificar duas ou mais proteínas, com funções distintas e algumas vezes até antagônicas, aumentando consideravelmente a capacidade codificante do genoma.
Esse splicing alternativo, descoberto independentemente em 1977 por Richard Roberts do New England Biolabs, nos EUA, e Phillip Sharp, do Massachusetts Institute of Technology (Instituto de Tecnologia do Massachusetts, MIT), EUA, pode explicar a diferença entre o tamanho “modesto” do conjunto gênico da espécie humana e a elevada complexidade do proteoma (conjunto de proteínas de uma célula), termo criado em 1995 pelo pesquisador Marc Wilkins.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.
Perguntas relacionadas
Materiais relacionados
 18 pág.
18 pág.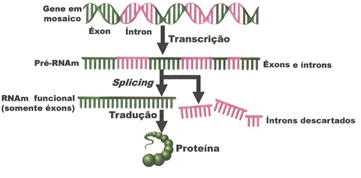







Compartilhar