Questão de Ciência dos Materiais, Resolva:
O Índio possui uma célula unitária tetragonal para a qual os parâmetros da rede a e c são 0,459 e 0,495nm, respectivamente. a) Se o fator de empacotamento atômico e o raio atômico valem 0,693 e 0,1625nm, respectivamente, determine o número de átomos em cada célula unitária. b) O peso atômico do índio vale 114,82g/mol; calcule sua massa específica teórica.
💡 2 Respostas
Julio C. Lourenço
Olá!
A célula unitária tetragonal consiste no seguinte desenho esquemático:
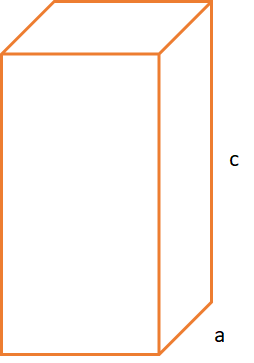
(a)
O fator de empacotamento é 0,693 e o raio atômico do índio vale 0,1625 nm. Os parâmetros de rede são: a = 0,459 nm e c = 0,495 nm.
Desta maneira teremos:
FEA = (nátomos x Volume) / Vcelula
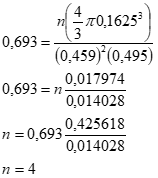
Resposta: O índio possui 4 átomos por célula unitária.
(b) Calcularemos inicialmente o peso de 4 átomos:
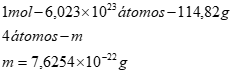
O volume em cm³ da célula unitária é:
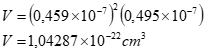
A massa específica teórica será então:
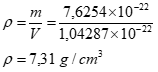
E esta é a resposta deste exercício!
Bons estudos!
Vagner Soares
a = 0,459 nm
c = 0,495 nm
FEA = 0,693
r = 0,1625 nm
Volume da celula = a²*c = 0,1043 nm³
FEA = (n*vol da esfera)/vol da celula
0,693 = (n*(4/3 * pi * 0,1625³)) / 0,1043
0,072271 = 0,017965n
n = 4 átomos
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Alguém poderia me ajudar com essa questão de Ciência dos Materiais.
Ciência dos Materiais
•UFMG
Marco Túlio Castro





Compartilhar