Relatorio de pratica (Padronização do HCl)
Alguem tem essa prática aí, de QUI200, Titulações, padronização do HCl?
Vlw
💡 3 Respostas
Neomara Mariani
Preparação e Padronização do HCl
2º Química
Prof. Valdir – Análise Química Quantitativa
Suzano, abril de 2013.
1.0 OBJETIVO
Preparar 100mL de uma solução aquosa de ácido cloridríco a 0,1mol/L a partir do ácido concentrado e padroniza-la com padrão primario carbonato de sódio usando indicador alaranjado de metila.
2.0 INTRODUÇÃO
A padronização da solução de ácido preparada é feita pela volumetria ácido-base, chamada acidimetria, usando-se uma técnica de laboratório chamada titulação, onde uma substância padrão-primário (substância não higroscópica, de alta pureza, que reage instântanea e completamente com o soluto da solução a ser padronizada) fica dissolvida em água no erlemmeyer com um indicador acido-base, enquanto que, na bureta, fica a solução ácida (solução-problema) cuja concentração real será determinada mediante a adição da mesma sobre o conteúdo do erlenmeyer, ate que uma gota em excesso faz a viragem do indicador, isto é, o indicador que é uma substância colorida, mua de cor à mudança de pH decorrente da pós- neutralização do padrão-primário.
3.0 PROCESSOS EXPERIMENTAL
3.1 Equipamentos Utilizados:
Balança Analítica
Suporte Universal
Balão Volumétrico
Bastão de Vidro
Béquer
Bureta
Erlenmeyer
Proveta
3.2 Reagentes Utilizados:
Água destilada
Ácido Cloridrico
Carbonato de Sódio
Bicarbonato de Sódio
Alaranjado de Metila
3.3 Procedimento
Preparo da solução de HCl
Primeiramente realizou-se os cálculos para preparar uma solução de HCl com concentração de 0,1Molar, considerando tambem o P.A de 37% presente no ácido clorídrico utilizado de acordo com o informado no rótulo do mesmo, considerou-se tambem a densidade do produto.
Após efetuar os cálculos, levou-se até a capela o vidro contendo o ácido clorídrico, adicionou-se uma pequena quantidade de água ao balão volumétrico utilizando a pisseta, logo após, pipetou-se a quantidade desejada de ácido e despejou-se no balão, depois completou-se com água destilada até o menisco do balão, fechou-se o mesmo e foi feita a homogenização.
Padronização da solução de Na2CO3
Pesamos o Carbonato de Sódio em um béquer de 100 mL na balança, deixando seu peso entre 0,1100 g e 0,1300 g e em seguida anotamos na ficha de controle de laboratório; adicionamos aproximadamente uns 15 mL de água destilada e agitamos até a completar a dissolução, feito isso, transferimos a solução titulante para um erlenmeyer de 250 mL, lavando o béquer três vezes com água destilada, após transferirmos a solução gotejamos quatro gotas de alaranjado de metila. A solução apresentou a cor laranja.
Titulação
Para realizarmos a titulação, lavou-se a bureta a ser utilizada, verificou-se a sua vazão e logo após ambientalizou-se a bureta com o ácido cloridríco, montou-se a parelhagem fixando a garra no suporte universal, adicionou-se o ácido a bureta ate completar seu traço, fixou-se a garra, e colou-se o erlenmeyer em baixo. A titulação foi feita até a viragem, anotou-se o volume usado para a padronização.
Logo após fez-se os cálculos da molaridade real das soluções e calculou-se também o fator de correção.
(Todos os procedimentos foram repetidos por cada integrante do grupo)
4.0 TRATAMENTO DE DADOS
Calculo da massa de HCl necessária para preparar o ácido a 0,1M
M x V = mM → 0,1 = m36,5 X 0,1 → m = 0,365g
Calculo da molaridade real:
Mr= 2 x mV gasto x M
1º Mr = 2 x 0,11040,0208 x 106 → 0,22082,2048 → Mr = 0,1001
Fc= 1,001
2º Mr = 2 x 0,11270,0210 x 106 → 0,22542,268 → Mr = 0,0994
Fc= 0,994
3º Mr = 2 x 0,11510,0215 x 106 → 0,23022,279 → Mr = 0,1010
Fc=1,010
4º Mr = 2 x 0,12230,0225 x 106 → 0,24462,385 → Mr = 0,1026
Fc= 1,026
5.0 RESULTADOS E DISCUSSÕES
Os resultados obtidos foram satisfatórios, já que o fato de correção deveria ser o mais proximo de 1,000. Todas as amostras não possuiram uma variante muito grande. Essa variante pode ter ocorrido pela quantidade a mais de soluto ou de solvente, outra explicação razoável para esse resultado pode ser a concentração do ácido clorídrico estava abaixo de 37%.
6.0 CONCLUSÃO
De acordo com os resultados obtidos conclui-se a importância da padronização de soluções, para verificar a concentração da mesma, pois podem apresenar variações, o que pode alterar resultados de experimentos realizados com a mesma.
Patrícia Luz
Padronização de soluções de NaOH 0,1 mol.L-1 e HCl 0,1 mol.L-1
Padronização de uma solução de NaOH
- Carregar uma bureta de 50 mL com a solução de NaOH 0,1 mol L-1 preparada na aula anterior.
- Pesar _____ g de biftalato de potássio e transferir para um erlenmeyer.
- Dissolver o sólido em 50 mL de água (esse volume de água tem que ser exato?) e adicionar 5 a 7 gotas de solução de fenolftaleína.
- Titular com adição lenta da solução de hidróxido de sódio até o ponto de viragem do indicador.
- Anotar o volume gasto.
- Fazer a determinação em triplicata.
- Calcular a concentração da solução de NaOH.
Reação entre o biftalato de potássio e o hidróxido de sódio
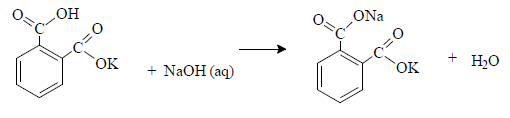
HOOCC6H4COOK(aq) + NaOH(aq) → NaOOCC6H4COOK(aq) + H2O(liq)
Padronização de uma solução de HCl
- Carregar uma bureta de 50 mL com a solução de NaOH 0,1 mol L-1 padronizada na etapa anterior.
- Transferir, 10 mL de HCl com exatidão (pipeta volumétrica) para um erlenmeyer de 250 mL e adicionar de 5 a 7 gotas de indicador fenolftaleína.
- Titular com adição lenta da solução de hidróxido de sódio até o ponto de viragem do indicador.
- Anotar o volume gasto.
- Fazer a determinação em triplicata.
- Calcular a concentração da solução de HCl.
Reação entre o ácido clorídrico e o hidróxido de sódio
HCl(aq) + NaOH(aq) → NaCl(aq) + H2O(liq)
Patrícia Luz
Solução 1 à Preparo da Solução de HCl 0,1mol/L:
Materiais utilizados:
- Balão Volumétrico 250ml;
- Pipeta Graduada 2ml;
- Pipeta Graduada 1ml;
- Pipetador manual;
- Água destilada;
- Ácido Clorídrico; ]
- Frasco grande;
Procedimento experimental:
Pegamos um balão volumétrico de 250ml para preparar tal solução seguindo os seguintes passos:
1º Passo: Calculo do volume de HCl necessário para preparar a solução:
Molaridade = 0,1
Massa = ? 0,9125
Massa Molar = 36,5 g/mol
Volume = 250ml = 0,25L
Densidade = 1,19g/mol Dado oferecido pelo professor.
Molaridade = massa
Massa molar x Volume
0,1 = massa / 36,5 x 0,250
Massa = 0,9125g
d = m/v
1,19 = 0,9125 / V
V = 1,08ml
1,08ml = 37% “dado oferecido pelo professor”
? = 100%
37? = 108
? = 2,9189ml
2º Passo: Preparo da solução após o calculo, com o resultado de 2,9189ml em mãos:
2,9789ml de ácido clorídrico é o volume necessário para o preparo da solução, portanto chegando a tal resultado, com uma pipeta, e dentro da capela com os óculos de proteção e as luvas devidamente colocadas nas mãos, pipetamos 2,1ml de HCl em duas etapas: a primeira com a pipeta de 2ml e a segunda com a pipeta de 1ml. Pipetamos o conteúdo necessário. Transferimos o conteúdo para o interior de um balão volumétrico de 250ml no qual já continha aproximadamente 150ml de água destilada. Completamos o balão volumétrico com água destilada até o menisco. Fechamos o balão volumétrico e homogenizamos a solução. Transferimos o conteúdo do balão volumétrico para um frasco devidamente rotulado HCl.
Solução 2 à preparo da solução NaOH 0,1mol/L:
Materiais utilizados:
- Balão volumétrico de 250ml;
- Béquer de 100ml;
- Água destilada;
- Bastão de Vidro;
- Balança;
- Balão volumétrico de 250ml
- Espátula;
- Hidróxido de sódio;
- Frasco Grande.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.







Compartilhar