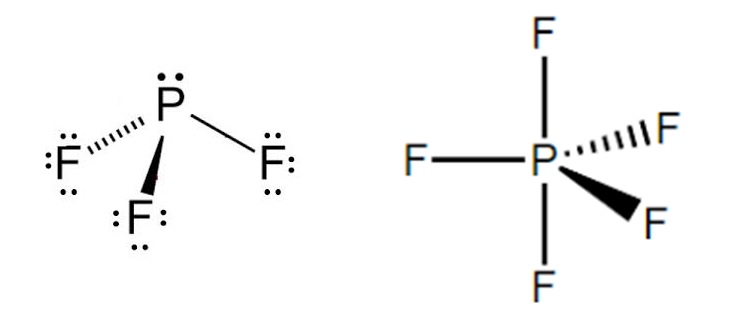
o fósforo forma dois fluoretos estáveis pf3 e pf5
A) utilizando a TLV mostre a formação desses fluoretos.
B) explique utilizando a TLV a formação do NF3. Existe a molecula NF5.
💡 2 Respostas
Especialistas PD
O fósforo forma dois fluoretos estáveis, PF3 e PF5, segundo a TLV, o número de orbitais híbridos requeridos por um átomo em uma molécula ou em um íon é determinado pela geometria dos pares de elétrons em torno desse átomo. Um orbital híbrido é necessário para cada ligação ou par de elétrons isolados no átomo central.
Distribuição eletrônica: P - 1s2 2s2 2p6 3s2 3p3
N - 1s2 2s2 2p3
O fósforo, pode formar tanto moléculas como o PF3 e PF5, uma vez que o mesmo apresenta 9 orbitais disponíveis em sua terceira camada de elétrons, podendo sofrer hibridização do tipo sp3, sp3d ou sp3d2.
O mesmo não acontece com o nitrogênio! Para formar moléculas, como NF5, ele deveria sofrer hibridização sp3d, e isso não é possível pois o mesmo não possui orbitais disponíveis em sua segunda camada de elétrons. Assim, o nitrogênio poderá sofrer apenas hibridização sp3, o que possibilitaria a formação somente da molécula NF3.
Pedro Lins
O fósforo tem acesso a orbitais d vazios, o que permite ele fazer algumas hibridações diferentes do nitrogênio.
O nitrogênio pode se hibridizar como, no máximo, sp3 e realizar uma ligação sigma com até três flúors, uma vez que um dos orbitais híbridos formados já está completamente preenchido.
O fósforo, por outro lado, pode se hibridizar como sp3d, utilizando um dos seus orbitais d da terceira camada. Sendo assim, ele forma cinco orbitais híbridos, cada um com um único elétron e portanto, pode realizar até cinco ligações sigma.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.
Perguntas relacionadas
Qual tipo de força atrativa intermolecular atua entre todas as moléculas?
Química Inorgânica I
•UNILAB
Helio Esperante




Compartilhar