porque a glicina não possui isomero ?
💡 3 Respostas
Ticianne Martins
Ticianne Martins
RD Resoluções
A isomeria óptica estuda o comportamento das moléculas ao receberem um feixe de luz polarizada. Algumas dessas moléculas têm a capacidade de desviar o feixe de luz, o que as caracteriza como opticamente ativas. Quando o plano da luz é desviado para a direita, é chamado de isômero dextrogiro e quando o plano é desviado pra esquerda, chamado de isômero levógero. Os isômeros possuem a mesma fórmula molecular, mas apresentam atividade óptica oposta e pode, resumidamente, ser identificado caso a molécula tenha um carbono quiral, ou seja, um carbono em que seus 4 ligantes sejam diferentes entre si. De todos os aminoácidos, o único que não possui isômero é a glicina.
Para entender o motivo da glicina não possuir isômero é importante lembrar que para apresentar isomeria, uma molécula precisa ter um carbono quiral, ou seja, que tenha 4 ligantes diferentes entre si. Ao observar a molécula da glicina (figura abaixo) é possível perceber que não há carbonos quirais. Um de seus carbonos está ligado a dois hidrogênios, o que gera um plano se simetria.
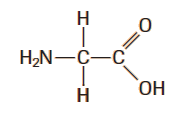
A glicina não apresenta carbonos assimétricos (quiral), dessa forma, não possui isômeros.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta






Compartilhar