explique a interação de substancias anfipaticas com a agua que tipos de estruturas supramoleculares podem ser formadas
💡 2 Respostas
RD Resoluções
Uma molécula anfipática é uma molécula que possui uma parcela hidrofílica (polar, denominada cabeça) e uma parte hidrofóbica (apolar, denominada cauda).
Um exemplo de substância anfipática é o surfactante comum (detergente), produto de limpeza amplamente utilizado. Você já deve ter percebido a formação de bolhas a partir dessa substância quando em contato com a água. A explicação para tal fenômeno é dada pelas interações que ocorrem entre cada parte da substância antipática em questão e a água. Veja:
Quando uma substância anfipática é mergulhada em água, a sua parcela hidrofílica (cabeça) procura reagir o máximo possível com água. Em contraposição, a parte hidrofóbica (cauda) procura um meio de se isolar do contato com o solvente. Neste caso, inúmeras moléculas da substância anfipática agregam-se numa configuração pelicular: uma estrutura arredondada, de forma que há encapsulamento das caudas, cercadas por uma camada de cabeças. Desta forma, tal estrutura é denominada micela. É o tipo mais comum de estrutura supramolecular formada nesta ocasião e também é responsável pela formação de bolhas no caso do detergente. Veja na imagem abaixo a representação gráfica da formação das micelas:
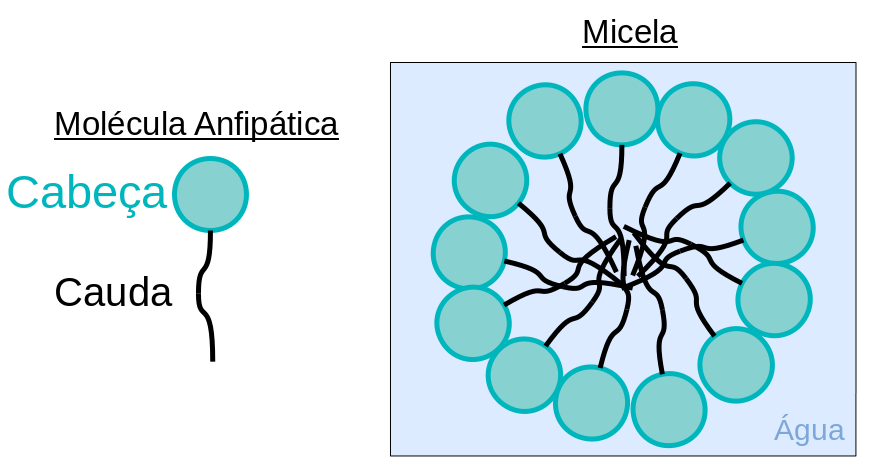
Fonte da Imagem: Criação Própria
thiago silva
vish
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.
Perguntas relacionadas
Materiais relacionados
 1 pág.
1 pág. 1 pág.
1 pág.





Compartilhar