O que não se sabia sobre o átomo até a década intermediária entre as duas grandes guerras mundiais do século passado?
I Guerra Mundial (1914 a 1918) II Guerra Mundial (1939 a 1945)
💡 3 Respostas
Wéslei Ribeiro
Procurando na internet achei este trecho de um site interessante que irá responder sua pergunta!
http://www.fem.unicamp.br/~em313/paginas/person/einstein.htm
Os fenômenos fotoelétricos apresentaram outra dificuldade para a teoria da radiação de Maxwell. Lord Rayleigh estimou em 1916 que, de acordo com Maxwell levaria horas para um elétron absorver energia de um feixe de radiação suficiente para desligar-se de um átomo. Mas Elster e Geitel tinham observado que o aparecimento de fotoelétrons ocorria simultaneamente com a iluminação da superfície do metal. De fato, E. Lawrence e J. W. Beams, em 1928, descobriram que o tempo gasto entre a incidência da radiação e o aparecimento de fotoelétrons era menor que 3x10-9 segundos. Se o efeito fotoelétrico era iniciado pela colisão de dois corpúsculos, o elétron e o fóton, então não há dificuldade para entender o caráter instantâneo da emissão.
O sucesso da hipótese do fóton em unificar a equação de Einstein (6) e em interpretar outros fenômenos fotoelétricos contrasta com a aplicação da teoria ondulatória da radiação ao campo de interferência e os efeitos de difração. Conclui-se que um duplo caráter deve ser associado à radiação e que uma descrição completa da sua interação com a matéria não pode ser obtida pelo uso consistente nem de uma teoria ondulatória nem de uma teoria corpuscular.
Rômulo C Ar
Tem mais, porém sua resposta é satisfatória e merece ser aprovada!
Abçs
Especialistas PD
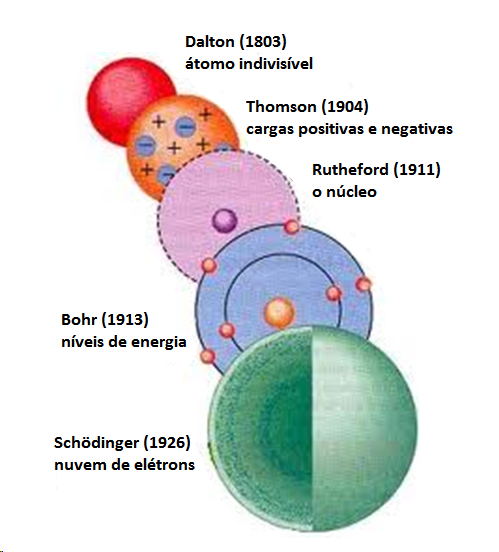
Em 1926, Heisenberg mostrou que não se pode determinar com exatidão a posição de um elétron, substituindo o conceito de posição por probabilidade de posição. Em 1927, Schrödinger conseguiu adaptar ao elétron a teoria de Heisenberg e outros. Utilizando equações de movimento de ondas, conseguiu deduzir equações matemáticas que determinam regiões no espaço onde temos a máxima probabilidade de encontrar determinado elétrons. Esta região é chamada orbital.
Não temos mais a ideia de que os elétrons são “bolinhas” em movimento rápido, girando em torno do núcleo. De acordo com esse novo modelo atômico, o elétron é uma partícula-onda que se movimenta no espaço, mas estará localizado com maior probabilidade no orbital. Devido à sua velocidade, o elétron permanece dentro do orbital, assemelhando-se a uma nuvem eletrônica.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.
Perguntas relacionadas
Materiais relacionados
 1 pág.
1 pág.Centro Educacional Dinamico
Vanubia Aguiar






Compartilhar