Compostos de Coordenação
As soluções de [Co(NH3)6]2+, [Co(H2O)6]2+ e [CoCl4]2- (tetraédrico) são coloridas. Uma é vermelho, uma é azul e outra é amarela. Especifique uma cor para cada complexo e justifique.
💡 3 Respostas
Letícia SSantos
Especialistas PD
[Co(NH3)6]2+ Amarelo
[Co(H2O)6]2+ Vermelho
[CoCl4]2- Azul
Segundo a TCC, Teoria do Campo Cristalino, a transição d-d é a origem de grande parte das cores dos complexos. E a cor depende da magnitude de Δ, se Δ é pequeno, baixa energia, absorve na região do vermelho e enxergamos a cor complementar, que é verde. Se Δ é grande, alta energia, absorve luz violeta e enxergamos a cor amarela. Podemos observar melhor na figura.
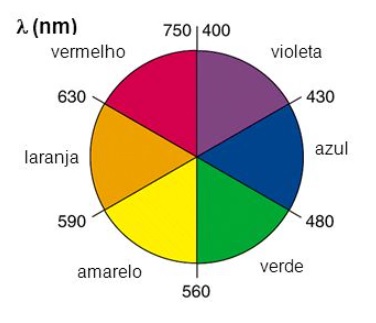
O [CoCl4]2- é tetraédrico e o Cl- é um ligante de campo fraco, então a solução é azulada, pois absorve na região próximo ao vermelho.
Os complexos [Co(NH3)6]2+ e [Co(H2O)6]2+ são octaédricos e o [Co(NH3)6]2+ possui ligante, NH3, de campo mais forte que a água do [Co(H2O)6]2+ (observar a série espectroquímica: I- < Br- < S2- < Cl- < NO3- < F- < OH- < EtOH < oxalato < H2O < EDTA < (NH3 e piridina) < etilenodiamina < bipiridina < o-fenantrolina < NO2- < CN- < CO), assim apresenta transição eletrônica de maior energia, absorvendo na região próxima ao azul, resultando em uma solução amarela.
Felipe Silva
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.
Perguntas relacionadas
Materiais relacionados
 10 pág.
10 pág.IFRJ - Instituto Federal De Educacao Ciencia E Tecnologia Do Rio De Janeiro Campus Eng Paulo De Frontin
Juliana Castro
 11 pág.
11 pág. 1 pág.
1 pág.




Compartilhar