o fosgênio cl2co tem um momento dipolo menor que o formaldeido, h2co, embora contenha átomos eletronegativos de cloro no lugar dos átomos de hdrogenio
💡 2 Respostas
Iara Oliveira
A determinação da polaridade de uma molécula pode ser realizada por meio do Momento de Dipolo ou Momento Dipolar Resultante, cujo símbolo é 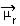 . Se estivermos falando apenas do momento dipolar de cada ligação da molécula, nesse caso o símbolo é a letra grega mi (µ).
. Se estivermos falando apenas do momento dipolar de cada ligação da molécula, nesse caso o símbolo é a letra grega mi (µ).

A molécula será apolar se o momento dipolar for igual a zero, mas se for diferente de zero, significa que ela é polar.

Existem duas coisas importantes a se considerar na determinação desse momento dipolar resultante. Vejamos quais são:
1) Diferença de eletronegatividade entre os átomos dos elementos participantes da reação. Por exemplo, a molécula de HF apresenta uma acentuada diferença de eletronegatividade, pois o flúor atrai, muito mais que o hidrogênio, o par de elétrons da ligação. Dessa maneira, a distribuição das cargas não é simétrica, apresentando dipolos elétricos.
Esse dipolo é representado por um vetor que fica virado para a extremidade que concentra mais os elétrons, ou seja, do átomo menos para o mais eletronegativo. Assim, nesse caso, o vetor, que é o único, será o vetor resultante, conforme indicado abaixo:
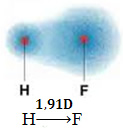
Observe que o valor do vetor é o mesmo do momento dipolar, que é dado na unidade debye (D= 3,33 . 10-30 coulomb . metro). Visto que o momento dipolar é diferente de zero, a molécula e a ligação são polares.
Estudante PD
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta




Compartilhar