Equacione a dissociação do ácidos
Equacione a dissociação do ácido acético em meio aquoso, apresente a expressão da constante de dissociação e justifique a variação do pH quando acetato de sódio é adicionado ao sistema ?
💡 2 Respostas
Inês Sousa Conde
CH3COOH (aq) ---> CH3COO- (aq) + H+ (aq)
K= ([CH3COO-][H+])/[CH3COOH]
RD Resoluções
Primeiramente a dissociação do ácido acético em soluçã o aquosa é:
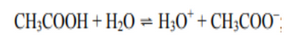
As constantes Ka e Kb , são representadas por:

Observando o va lor de Ka e K b concluímos portanto, que se trata de um ácido relativamente forte(ácidoacético) com uma base conjugada relativamente fraca (acetato de sódio) . Quanto ao pH da so lução depois do acréscimo do acetato de sódio , podemos dizer que este tende a aumentar muito pouco , devido a compensação do consumo de ácido acético pela reação de hidrólise da base conjuga da do ácido que é o íon acetato , formando íons de ácido acético.
fonte:http://www.quimica.ufpr.br/nunesgg/CQ108/Eqilibrio%20em%20solu%C3%A7%C3%A3o%20aquosa/solucao%20tampao.pdf
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta




Compartilhar