indique quais das seguintes especies poden formar ligações de hidrogenio com a agua
💡 2 Respostas
Carol Prates Loriato
As forças intermoleculares, como o próprio nome diz, são as forças que mantêm as moléculas de uma substância unidas.
Estas forças são chamadas também de forças de Van der Waals em homenagem ao físico holandês Johannes Van der Waals (1837-1923), que pesquisou e propôs a existência destas forças.
Entre estas forças, as que têm intensidades mais elevadas são as Ligações de Hidrogênio. Este tipo de interação ocorre quando a molécula possui um hidrogênio (“polo positivo”) ligado ao flúor, nitrogênio ou oxigênio, ou seja, elementos muito eletronegativos (“polos negativos”).
Como esta força é muito forte, origina dipolos muito acentuados; e é necessária uma energia muito alta para romper as moléculas.
As ligações de hidrogênio existem entre as moléculas de água. Observe a figura abaixo:
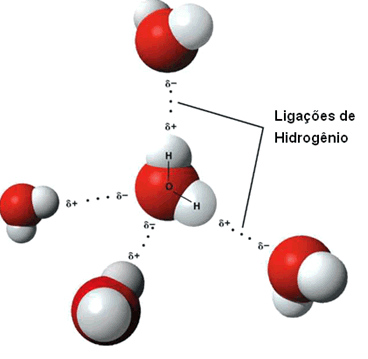
Ligações de hidrogênio entre as moléculas de água
Pode-se observar que o hidrogênio (carga positiva) atrai o oxigênio (carga negativa) das moléculas de água vizinhas. Assim, ocorre a ligação de hidrogênio, onde cada molécula de água fica circundada por outras quatro moléculas de água.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.




Compartilhar