Explique a diferença de velocidade de reação e equilíbrio da reação.
💡 2 Respostas
medicamentos ufrn
A velocidade refere-se ao tempo no qual aquela reação irá ocorrer. O equilíbrio representa o instante em que a quantidade de reagentes serão iguais aos produtos.
RD Resoluções
Um dos fatores que interferem na velocidade, rapidez ou taxa de desenvolvimento de uma reação química é a concentração dos reagentes. Conforme dito no texto “Influência da Concentração na Velocidade das Reações”, geralmente, um aumento na concentração dos reagentes aumenta a rapidez de uma reação.
Isso pode ser visto na reação de decomposição da água oxigenada (solução aquosa de peróxido de hidrogênio):
H2O2(l) → H2O(l) + ½ O2(g)
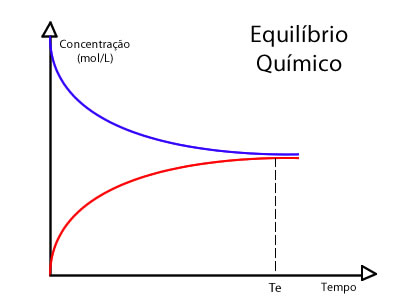
As reações direta e inversa ocorrem em velocidades diferentes, mas tendem a se igualar. Quando ambas as velocidades das reações direta e inversa se tornam iguais, e, portanto, as concentrações de todas as substâncias da reação permanecem constantes, diz-se que a reação atingiu seu equilíbrio químico.
Quando uma reação reversível atinge o equilíbrio químico, a relação dos produtos e reagentes é constante (o que não quer dizer que isso ocorra em proporção de 1 : 1 necessariamente), o que recebe o nome de constante de equilíbrio. A constante de equilíbrio pode ser expressa em termos das concentrações em mol/L (Kc), em que não entram os sólidos, ou em termos de pressão parcial (Kp), em que somente os gases participam.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.




Compartilhar