Como realiza o calculo de balanceamento de Oxidorredução?
💡 1 Resposta
RD Resoluções
As reações de oxirredução envolvem a transferência de elétrons entre átomos, íons ou moléculas.
Em uma reação de oxirredução ocorrem mudanças no número de oxidação (nox). A oxirredução consiste nos processos de oxidação e redução:
Oxidação: Resulta na perda de elétrons e aumento do nox.
Redução: Resulta no ganho de elétrons e diminuição do nox.
Ao mesmo tempo que um elemento cede elétrons, outro irá recebê-los. Assim, o número total de elétrons recebidos é igual ao total de elétrons perdidos.
Conforme o elemento que recebe ou doa os elétrons temos as seguintes denominações:
- Agente Redutor: Aquele que sofre oxidação, provoca a redução e aumenta o seu número de nox. É o que perde elétrons.
- Agente Oxidante: Aquele que sofre redução, provoca a oxidação e diminuiu o seu número de nox. É o que ganha elétrons.
O numero de oxidação representa a carga elétrica de um elemento no momento em que participa de uma ligação quimica.
Essa condição é relacionada com a eletronegatividade, que é a tendência que alguns elementos apresentam para receber elétrons.
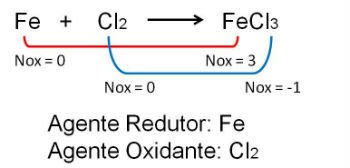
1. Observe o primeiro exemplo, note que na reação entre o Ferro e o Cloro ocorre mudança do número de oxidação. O Cloro por ser mais eletronegativo ganha elétrons:
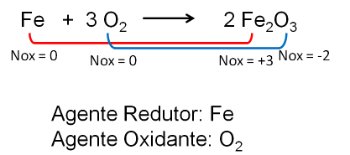
2. Reação entre o Ferro e o Oxigênio. O oxigênio é mais eletronegativo e acaba por receber elétrons e diminuindo o seu número de oxidação.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.
Perguntas relacionadas
Qual a importância das reações de oxidorredução em um processo?
Bioquímica Aplicada à Farmácia
•Unifael
Stefanie Grando
Materiais relacionados
 7 pág.
7 pág.




Compartilhar