verdadeiro ou falso?
💡 2 Respostas
Vinicius Freitas
Acho que pra responder teria que ter a entalpia de combustão do metano, não?
Passei Direto
A massa de metano queimada (6,9 g) libera 350 kJ.
Para realizarmos esse cálculo é necessário sabermos os valores de entalpia de formação das substâncias envolvidas na queima do metano (ver tabela).
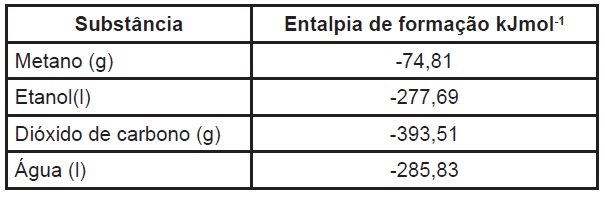
A combustão (queima) do metano, se dá pela equação: CH4 + 2 O2 → CO2 + 2 H2O. Calculamos a variação de entalpia para a combustão do metano: ΔH = Hprodutos - H reagentes
ΔH = [(2 x HH2O) + (HCO2)] - [(HCH4)]
ΔH = [2 x (-285,83) + (-393,15)] - [(-74,81)]
ΔH = - 890,36 kJ/mol
Que significa dizer que cada mol de metano queimado, libera 890,36 kJ de energia! Um mol de metano tem massa molar de 16g. Então a queima de 16 gramas libera 890,36 kJ de energia. Para 350 kJ (conforme enunciado) será necessária qual massa? Resolvendo a regra de três, temos que 6,29 gramas de metano liberam 350 kJ de energia. Então é verdadeiro!
16 g ---------- 890,36 kJ
x ---------- 350 kJ
x = 6,29 g de metano.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.




Compartilhar