balanço de massa com reaçoes quimicas
análise de um carvão indica, em porcentagens mássicas, 75% de C, 17% de H, 2% de S e o balanço cinzas não combustíveis. O carvão é queimado a uma taxa de 5000 kg/h, e a taxa de alimentação de ar à fornalha é 75 kmol/min. 6% do C do combustível não sofre combustão. Toda a cinza e o C não queimado deixam a fornalha como uma escória fundida. O carbono queimado forma CO2 e CO, o enxofre forma SO2 e o H do carvão é oxidado a água. A seletividade de CO2 para CO é 10:1.
a-) Calcule a porcentagem de excesso de ar no reator.
b-) Calcule a fração molar dos gases poluentes CO e SO2 no gás de chaminé
💡 2 Respostas
Rafael Izidoro
A)
Proporção estequiométrica considerando a seletividade:

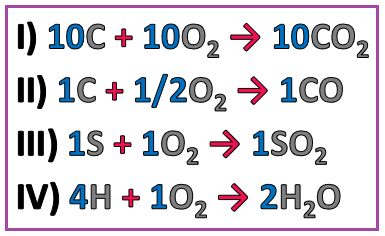
Combustíveis no carvão:
Carvão = 5000 kg/60min = 83,33 kg/min

C = 75% . 94% . 83,33 kg/min = 58,74765 kg/min
S = 2% . 83,33 kg/min = 1,666 kg/min
H = 17% . . 83,33 kg/min = 14,1661 kg/min
Consumo molar de combustíveis e O2 no reator:

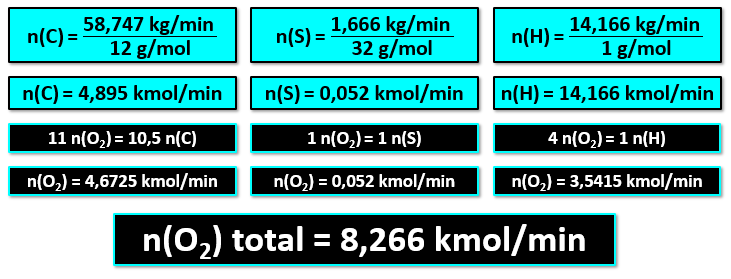
Sabendo que o ar é constituído por 20% (em mols) de O2:

Sobra de ar:

Percentual molar de ar não consumido (excesso):

Filipe Bento
co2
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.
Perguntas relacionadas
Materiais relacionados
 12 pág.
12 pág.




Compartilhar