consentração normal
Foram dissolvidos 16,987 g de nitrato de prata em 100 mL de água destilada. A solução foi transferida para balão volumétrico de 500 mL, o volume completado e a solução homogeneizada. Qual é a concentração normal da solução final?
💡 2 Respostas
João Vítor
É só dividir a massa pelo volume: d=m/V
Que resulta em 0,033974g/ml
Especialistas PD
A concentração normal da solução final (normalidade) é a relação entre o equivalente-grama do soluto e o volume da solução. A unidade é representada pela letra N (normal). Está em desuso, mas ainda pode ser encontrada em alguns rótulos nos laboratórios.
N = nEq / V
Onde, N = normalidade (N), nEq = número de equivalente-grama do soluto e V = volume da solução
Para calcularmos o equivalente-grama de um sal, basta dividirmos a massa molar (MM), pelo número de elétrons transferidos.
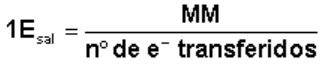
Então para o nitrato de prata, de fórmula AgNO3 (MM = 169,87 g/mol), temos: AgNO3 → Ag+ + NO3- , o número de elétrons transferidos é 1.
E = 169,87 / 1 = 169,87
E é dito no enunciado que foram colocados 16,987 g de nitrato de prata, então temos:
1E ------- 169,87
x ------- 16,987
x = 0,1
Se N = nEq / V, onde o V em litros é de 500 mL = 0,5 L
N = 0,1/0,5 = 0,2 N
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.




Compartilhar