O pH de una solução 0,012M de uma base,BOH, foi determinado experimentalmente como sendo igual a 11,40.Calcule o Kb da base.
💡 3 Respostas
Andre Smaira
A definição de pH assume a seguinte relação:
$$pH+pOH=14$$
Tendo que o valor de pOH é de 2,6.
O pOH é definido por:
$$pOH=-\log [OH^-]$$
$$[OH^-]=10^{-2,6}=0,0025$$
Conhecendo a equação química para dissociação do BOH:
$$BOH\leftrightarrow +[B^+]+[OH^-]$$
Tem-se:
$$[OH^-]=0,0025$$
$$[B^+]=0,0025$$
$$[BO]=0,012-0,0025-0,0025=0,007$$
Assim, o valor de Kb é dado por:
$$K_b=\dfrac{[B^+][OH^-]}{[BO]}=0,000893$$
Dessa forma, o valor de Kb é de 0,000893.
RD Resoluções
A definição de pH assume a seguinte relação:
$$pH+pOH=14$$
Tendo que o valor de pOH é de 2,6.
O pOH é definido por:
$$pOH=-\log \[OH^-\]$$
$$\[OH^-\]=10^{-2,6}=0,0025$$
Conhecendo a equação química para dissociação do BOH:
$$BOH\leftrightarrow +\[B^+\]+\[OH^-\]$$
Tem-se:
$$\[OH^-\]=0,0025$$
$$\[B^+\]=0,0025$$
$$\[BO\]=0,012-0,0025-0,0025=0,007$$
Assim, o valor de Kb é dado por:
$$K_b=\dfrac{\[B^+\]\[OH^-\]}{\[BO\]}=0,000893$$
Dessa forma, o valor de Kb é de 0,000893.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.
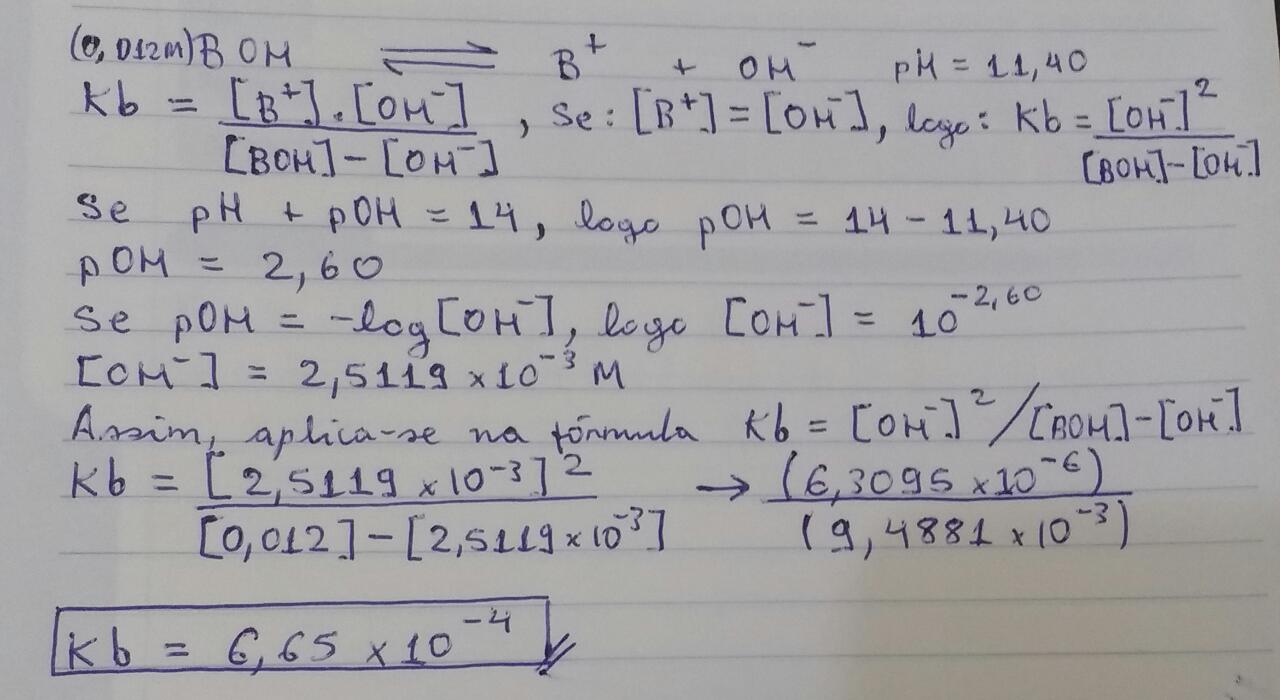




Compartilhar