Biofísica Água e soluções.
Um pesquisador precisa preparar 100 mL de uma solução de MgCl2 0,1 M. A receita para o preparo desta solução pede que seja pesado 0,94 g deste sal. No entanto, no laboratório este dispõe apenas de MgCl2.6H2O. É correto usar a mesma massa deste último para se preparar a solução em questão? Caso contrário, que correções devem ser feitas a qual a massa necessária do sal disponível no laboratório? Dados massas atômicas: Mg: 24, Cl: 35, H: 1, O: 16.
(OBS: já fiz a questão, só não sei a resposta)
💡 4 Respostas
Maria Luisa
Andre Smaira
Vamos usar conceitos de química geral e operações básicas de matemática para resolvermos o problema.
Como o sal que o laboratório dispõe é hexa-hidratado, obviamente devemos considerar a massa de água presente para obtermos a concentração exigida.
A massa molar do sal 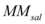 é dada:
é dada:
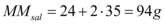
Já para o sal hidratado temos a massa molar 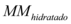 :
:
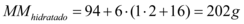
Ou seja, a cada grama que pesamos do sal hidratado, temos 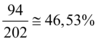 do sal puro. Desta forma, usando a regra de três, podemos encontrar a massa
do sal puro. Desta forma, usando a regra de três, podemos encontrar a massa  do sal hidratado a ser pesada:
do sal hidratado a ser pesada:
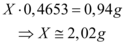
Portanto, a massa do sal disponível necessária para preparo da solução é de 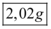 .
.
Andre Smaira
Vamos usar conceitos de química geral e operações básicas de matemática para resolvermos o problema.
Como o sal que o laboratório dispõe é hexa-hidratado, obviamente devemos considerar a massa de água presente para obtermos a concentração exigida.
A massa molar do sal é dada:
Já para o sal hidratado temos a massa molar :
Ou seja, a cada grama que pesamos do sal hidratado, temos do sal puro. Desta forma, usando a regra de três, podemos encontrar a massa
do sal hidratado a ser pesada:
Portanto, a massa do sal disponível necessária para preparo da solução é de .
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.







Compartilhar