20% dos átomos de cobre são substituídos por alumínio em um bronze de alumínio. Quais os percentuais em peso dos elementos em 100 átomos?
Peso atômico do cobre: 64 g/mol
Peso atômico do alumínio: 27 g/mol
💡 2 Respostas
Luiz Fernando Kultz Unti
Se tomarmos os 100 átomos solicitados, 20% dos átomos de Alumínio adicionados serão 20 átomos. Então, temos:
- Cobre: 80 átomos x PA cobre = 80 * 64 g/mol = 5.120 g/mol
- Alumínio: 20 átomos x PA alumínio = 20 * 27 g/mol = 540 g/mol
O peso total então seria, nos 100 átomos, 5.660 g/mol. Agora, com esse valor total, e os pesos parciais de cada elemento, basta fazer uma regra de três simples para encontrar a porcentagem procurada:
- Cobre: (5.120/5660)*100 = 90,46%
- Alumínio: (540/5.660)*100 = 9,54%
Espero ter ajudado. Boa sorte!
Julio C. Lourenço
Considere 0,8 mol de átomos de alumínio (80 %) e 0,2 mol de átomos de cobre (20 %). Estes pesariam juntos:
Peso = 0,8 * 27 + 0,2 * 64 = 34,4 g
Logo, esta liga deve pesar 34,4 g/mol.
Em seguida, temos para esta liga que:
1 mol = 6,023x1023 átomos = 34,4 g
Para 100 átomos faremos uma regra de três simples:
6,023x1023 átomos - 34,4 g
100 átomos - W
Que resulta em:
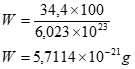
E esta é a resposta deste exercício.
Bons estudos!
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.
Perguntas relacionadas
1- Uma liga contém 80% em peso de alumínio e 20% de magnésio. Qual é a % atômica de cada um?
Ciência dos Materiais
•UVA
Myllana
Materiais relacionados
 3 pág.
3 pág. 2 pág.
2 pág. 2 pág.
2 pág.




Compartilhar