Como transformar concentração molar para ppm?
💡 2 Respostas
Allan Henric
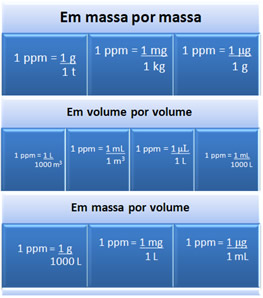
A concentração em ppm indica quantas partes do soluto existem em 1 milhão de partes da solução (em volume ou massa).

Especialistas PD
Para convertermos a concentração molar (mol/L) para ppm (partes por milhão), podemos estabelecer uma relação de massa.
ppm = 1 parte soluto/106 partes da solução
Se estamos falando em quantas partes de soluto em um milhão de partes de solvente, considerando esse solvente como a água, seriam partes em gramas de soluto para 1.000.000 g de solvente.
1.000.000 g = 1000 kg = 1000 L
Pegando a concentração molar, conseguimos calcular o número de mols para 1000 L (1.000.000 g), e daí obter a massa (n = m/MM) e já temos a resposta em ppm.
Por exemplo, qual a concentração em ppm de uma solução 0,001 mol/L de NaOH?
Temos 0,001 mol de NaOH em 1 L de solução = 1000 g. Em 1.000.000 g teremos 1 mol de NaOH. Calculando a massa molar do hidróxido de sódio, temos 40 g/mol. Então em 1 mol temos 40g, assim 40 g em 1 milhão de gramas. Ou seja, 40 ppm.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.





Compartilhar