quem tem a quinta maior energia de ionização C ou B?
💡 1 Resposta
Especialistas PD
Energia de ionização é a energia mínima necessária para remover um elétron de um átomo na fase gasosa.
O carbono, de menor raio atômico que o boro, possui a 1ª energia de ionização maior, pois como há maior atração do seu núcleo pelos elétrons, torna-se difícil a remoção do elétron, elevando o valor da energia de ionização, como podemos observar na tabela abaixo:
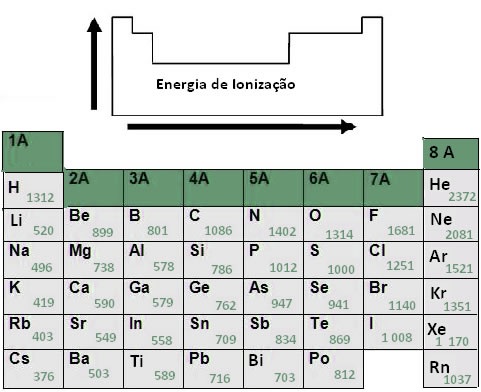
Para a 5ª energia de ionização, vammos analisar a distribuição eletrônica do carbono (Z=6) e do boro (Z=5).
C: 1s2 2s2 2p2
B: 1s2 2s2 2p1
Remover o quinto elétron (5ª energia de ionização) será mais difícil no átomo de boro, que possui 5 elétrons. Remover o quinto, seria remover seu último elétron, que estará fortemente atraído pelo núcleo positivo.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.
Perguntas relacionadas
QUAL o grau de ionização do ácido tartárico no pH 1,8 e pKa=2,98?
Química Geral Experimental
•Anhanguera
Darlene Silva
Materiais relacionados
 3 pág.
3 pág. 5 pág.
5 pág.




Compartilhar