O que é um orbital anti ligante?
💡 2 Respostas
Aldilene França
É o orbital que tende a desestabilizar a ligação
Especialistas PD
Na química, o orbital antiligante é um tipo de ligação química dada pela sobreposição de dois orbitais moleculares semi-preenchidos.
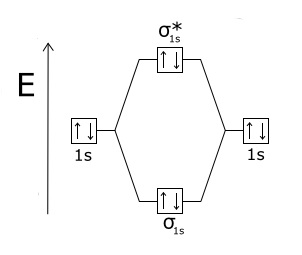
Um orbital de ligação molecular torna-se um orbital antiligante quando a densidade de elétrons entre os dois núcleos é menor do que aquela que seria se os dois núcleos fossem separados. Os orbitais antiligantes são rotulados com o asterisco (*) nos diagramas dos orbitais moleculares; estes derivam da sobreposição fora da fase de funções de onda e são caracterizados por uma maior energia em relação aos orbitais ligantes. No caso da molécula diatómica de hidrogénio (H2) cada átomo contribui para o orbital com um só elétron, portanto, apenas o orbital σ é preenchido e a molécula é mais estável dos dois átomos separados que a compõem.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta






Compartilhar