quimica analitica
Tendo como base o que foi estudado em sala de aula e o que norteia o efeito “Salting Out”. Explique o motivo de se usar um solvente orgânico para extrair íons metálicos de soluções inorgânicas no trecho abaixo retirado do livro “Fundamentos de Química Analítica”, p. 829:
“Extração de Cloretos e Nitratos de Metais
Inúmeras espécies inorgânicas podem ser separadas por meio de extração com solventes adequados. Por exemplo, uma extração simples em éter de uma solução 6 mol L-1 de ácido clorídrico vai proporcionar a transferência de mais de 50% de diversos íons para a fase orgânica; incluindo entre esses o ferro (III), o antimônio(V), o titânio (III), o ouro (III), o molibdênio (VI) e o estanho (IV). Outros íons, tais como o alumínio (III) e os cátions divalentes do cobalto, chumbo, manganês e níquel, não são extraídos. O urânio (VI) pode ser separado de elementos como o chumbo e o tório pela extração com éter de uma solução que seja 1,5 mol L-1 de ácido nítrico e saturada
com nitrato de amônio. O bismuto e o ferro (III) são também extraídos em alguma extensão nesse meio.”
💡 1 Resposta
ana yasmin gonçalves
bom eu aprendi algo parecido em gênese dos solos; as plantas secretam na parte da raiz acidos orgânicos para que haja a mobilização de Al, Fe, Mo, Ag, porque esse acido carboxilico (ali na imagem) é ligado a uma hidroxila, so que no processo de hidrolise esse H+ sai do Oh e protona o meio externo. essa acidificação do meio mobiliza esses ions metalicos para perto das raizes para que eles sejam incorporados. creio que no seu caso isso tbm seja verdade, ou seja, esse acido orgânico tem poder de agregar ions metalicos, justamente por causa da hidrolise da OH 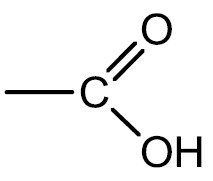
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.




Compartilhar