Por que no processo de zincagem do aço carbono pode ocorrer a oxidação do ferro?
💡 2 Respostas
Cássia Beatriz
O processo de zincagem é um processo de galvanização, porém o zinco apresenta maior potencial de oxidação que o ferro.
Não sei se entendi direito sua pergunta.
Especialistas PD
O ferro e o aço são materiais muito utilizados na produção de peças metálicas. No entanto, um aspecto negativo dos materiais feitos de ferro e de aço é que, com o tempo, eles se enferrujam e geram enormes prejuízos econômicos e ambientais. Para impedir ou pelo menos diminuir esses prejuízos, existem vários métodos de proteção contra a corrosão dos metais, sendo que um dos mais eficientes é a galvanização. A galvanização é um processo em que se reveste uma peça de ferro ou de aço com zinco metálico. Quando uma peça passa por um processo de galvanização, a camada de zinco impede a oxidação do ferro, porque evita que ele entre em contato com o ar e com a água.
Mas e se o objeto for riscado e o ferro entrar em contato com o ar úmido? Sem problemas, porque inicialmente o ferro se oxidará, mas imediatamente o zinco também se oxidará, pois como é mostrado abaixo, o potencial de redução do zinco é menor que o do ferro e do que o do oxigênio e da água. Portanto, a tendência do zinco em oxidar-se é maior.
Zn(s) → Zn2+ + 2e- E0redução = - 0,76 V
Fe(s) → Fe2+ + 2e- E0redução = - 0,44 V
O2 + 2 H2O + 4 e- → 4 OH- E0redução = + 0,40 V
Quando o zinco se oxida, acontecem duas coisas importantes que impedem o ferro de ser corroído. A primeira é que, visto que seu potencial de redução é menor que o do ferro, ele reduz o cátion Fe2+ a ferro metálico novamente:
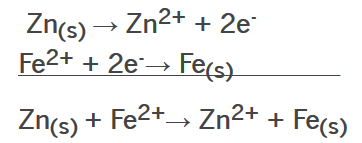
O segundo ponto é que, em contato com o ar e a água, o zinco origina o composto Zn(OH)2, que se deposita sobre o ferro que estava exposto e novamente o protege contra a corrosão.
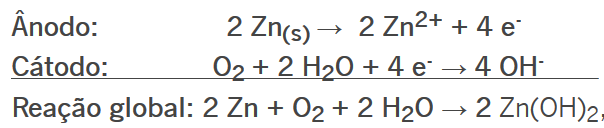
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.







Compartilhar