Monte o ciclo de Born-Haber para o fluoreto de cálcio CaF. Não esqueça de indicar todas as etapas envolvidas na formação desse sal.
💡 1 Resposta
Camila Assis
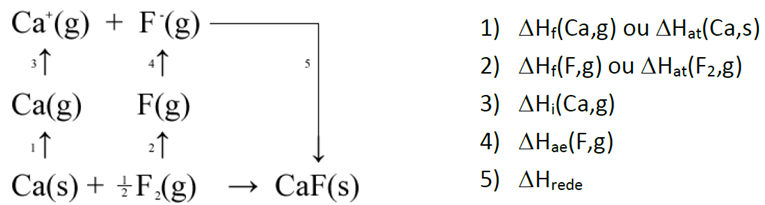
No ciclo de Bohr-Haber as energias envolvidas no caminho dos reagentes até os produtos correspondem à soma de todas as energias envolvidas no processo. Para determinarmos a energia reticular do CaF, um composto hipotético, temos que sua entalpia padrão de formação é igual à soma do ΔH da correspondente a passagem do cálcio sólido para gasoso, mais o ΔH de ionização do cálcio (formação do Ca+ no composto hipotético), mais o ΔH de dissociação da molécula diatómica de flúor, mais a afinidade eletrônica, para que o flúor na fase gasosa receba um elétron e por fim, mais a energia de rede. Através destes cálculos podemos predizer a existência ou não de um composto.
∆Hf°CaF,s= ΔHf(Ca,g) + ΔHf(F,g) + ΔHi(Ca,g) + ΔHae(F,g) + ΔHrede
Ficou curioso? Acesse o link https://www.passeidireto.com/video/45459403/ligacoes-ionicas-teoria
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.







Compartilhar