Extintores de incêndio à base de gás carbônico não podem ser usados para apagar fogo provocado por sódio metálico porque o gás carbônico...
reage com o metal aquecido, formando carbonato de sódio e carbono elementar.
a) Equacione esta reação;
b) Esta reação é de óxi-redução?
c) Identifique os agentes oxidante e redutor deste processo
💡 2 Respostas
Rafael Izidoro
A)


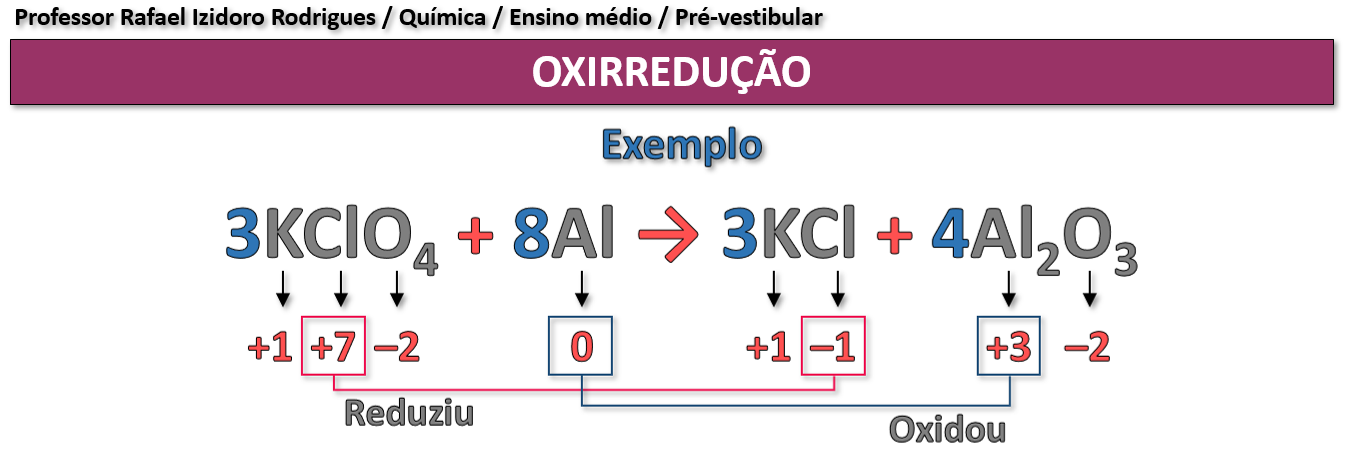
B) Sim.
Para que uma reação seja classificada como redox, deve haver variação de NOX!
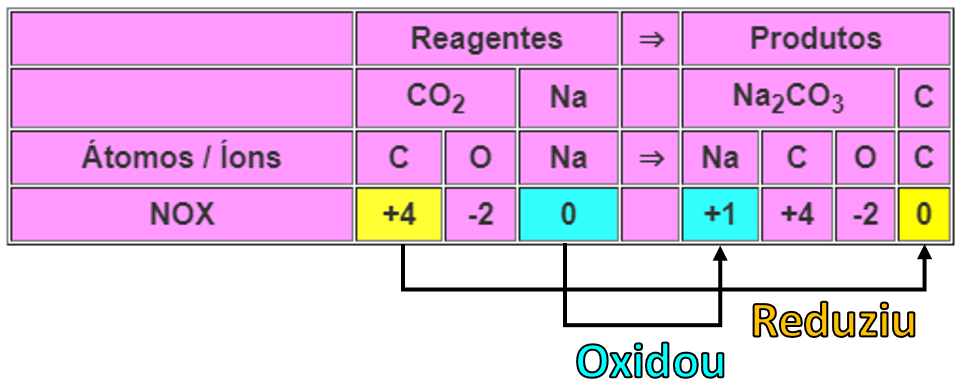
C) Sim.

Espécie que oxida: é redutora.
Espécie que reduz: é oxidante.

Acesse o material completo (slides) no google drive!
Camila Assis
a) A reação entre o sódio metálico (Na) com o gás carbônico (CO2) tem como produtos o carbonato de sódio (Na2CO3) e o carbono elementar (C), segundo a reação balanceada:
4 Na + 3 CO2 → 2 Na2CO3 + C
b) Esta é uma reação de oxirredução, já que envolve transferência de elétrons. O sódio possui número de oxidação (Nox) igual a zero nos reagentes e +1 nos produtos. Isso nos diz que ele perde um elétron (oxidação). Já o carbono, com Nox +4 nos reagentes passa a ser zero nos produtos, ganhando 4 elétrons (redução).
c) Como o Na é oxidado, ele força que outro se reduza, então é o agente redutor. Já o que sofreu a redução faz com que ocorra uma oxidação, então o CO2 é o agente oxidante.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 1 pág.
1 pág. 1 pág.
1 pág. 1 pág.
1 pág.




Compartilhar