UERJ 2014 - O ciclo do nitrogênio é extremamente importante para os seres vivos.
Esse elemento faz parte de diversos compostos orgânicos, como proteínas e ácidos nucleicos. Na tabela, há exemplos de formas químicas do nitrogênio incorporadas por alguns seres vivos.
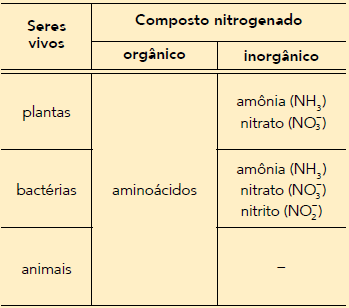
O nitrato, íon de geometria trigonal plana, serve como fonte de nitrogênio para as bactérias.
Observe as seguintes fórmulas estruturais:
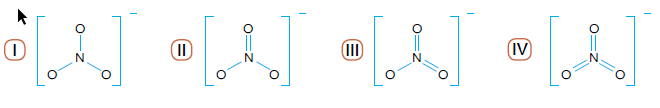
A fórmula que corresponde ao íon nitrato está identificada pelo seguinte número:
(A) I
(B) II
(C) III
(D) IV
💡 2 Respostas
Mateus Oliveira
Camila Assis
O íon nitrato possui fórmula NO3-. Através da posição na tabela periódica ou pela configuração eletrônica do nitrogênio e do oxigênio, sabemos quantos elétrons eles possuem na camada de valência (última camada eletrônica). O nitrogênio, família 15, possui 5 elétrons na última camada, e o O, família 16, 6 elétrons.
Segundo a regra do octeto, a qual diz que um átomo adquire estabilidade com oito elétrons em sua camada de valência, o nitrogênio irá formar uma ligação dupla com o primeiro dos átomos de oxigênio (que também ise estabilizará eletrônicamente) e uma ligação simples com um segundo átomo de oxigênio. Por ser um ânion de carga –1, o nitrato contém mais um elétron dos que os presentes nos átomos participantes. Esse elétron se liga ao segundo átomo de oxigênio, proporcionando assim sua estabilidade. Ainda resta o terceiro átomo de oxigênio, que necessita de dois elétrons para alcançar a estabilidade. Como o nitrogênio já completou sua última camada, uma ligação covalente dativa entre o nitrogênio e o terceiro oxigênio é formada, utilizando dois elétrons livres do átomo de nitrogênio.
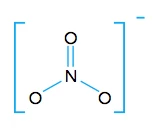
Gabarito: letra B
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.






Compartilhar