ITA 2003 - Uma mistura de azoteto de sódio, NaN3(c), e de óxido de ferro (III), Fe2O3(c), submetida a uma centelha elétrica reage muito
rapidamente produzindo, entre outras substâncias, nitrogênio gasoso e ferro metálico. Na reação entre o azoteto de sódio e o óxido de ferro (III) misturados em proporções estequiométricas, a relação (em mol/mol) N2(g)/Fe2O3(c) é igual a
A. ( ) 1/2. B. ( ) 1. C. ( ) 3/2.
D. ( ) 3. E. ( ) 9.
💡 1 Resposta
Camila Assis
Para resolvermos essa questão e encontrarmos a relação entre N2 e Fe2O3 temos que escrever a equação química:
NaN3 + Fe2O3 → N2 + Fe + ...
Temos uma reação de oxirredução e para o balanceamento podemos seguir alguns passos:
1º passo) Calcular o Nox de todos os elementos e determinar a variação do Nox (quem se reduz e quem se oxida).
2º passo) Calcular a variação total do Nox (Δ)
Δ = (variação do Nox do elemento) x (nº átomos do elemento na molécula).
3º passo) Tornar o Δ do oxidante como coeficiente do redutor e vice-versa.
Obs: Qual lado da equação usar o coeficiente?
- ao lado do elemento cujo Nox não se repete na equação;
- no elemento com maior atomicidade (maior número de átomos).
4º passo) Prosseguir o balanceamento pelo método das tentativas.
Determinando os nox:
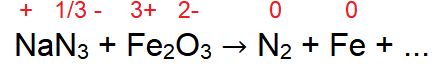
Observamos que o nitrogênio passa de nox - 1/3 para zero, temos uma oxidação, perda de elétrons. Δ = 1/3 x 3 = 1
Já o ferro passa de +3 para 0, uma redução, ganho de 3 elétrons. Δ = 3 x 2 = 6. Tornando o Δ do oxidante como coeficiente do redutor e vice-versa:
6 NaN3 + 1 Fe2O3 → N2 + Fe + ...
Prosseguindo o balanceamento pelo método das tentativas:
6 NaN3 + 1 Fe2O3 → 9 N2 + 2 Fe + ...
Então a relação (mol/mol) N2 / Fe2O3 = 9/1 = 9.
Gabarito: letra E
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta






Compartilhar