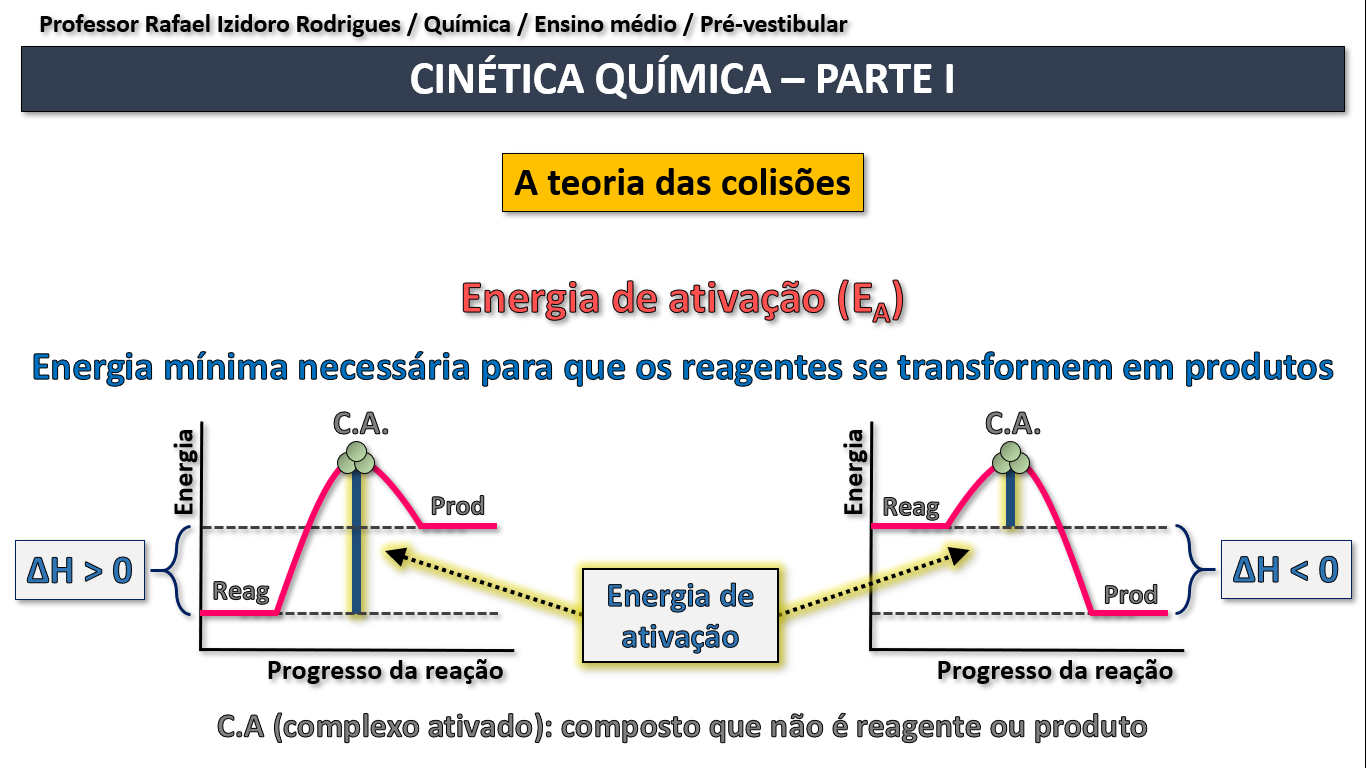
(UERJ 2018) Observe no gráfico os valores de entalpia ao longo do caminho de uma reação de hidrogenação do pent-2-eno, em duas condições:
presença e ausência de catalisador.
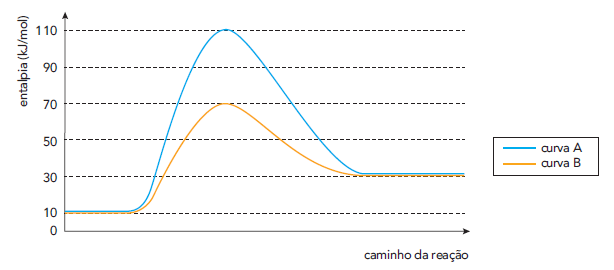
Indique a curva que representa a reação química na presença de catalisador e calcule, em kJ/mol, sua energia de ativação.
Determine, ainda, a variação de entalpia dessa reação, em kJ/mol, e nomeie o produto formado.
💡 3 Respostas
Celso Bortoletto
Energia de ativação = 70 – 10 = 60 kJ/mol
DH 30 – 10 = 20 kJ/mol
Nome do produto: Pentano.
Estudante PD
Quanto à reação catalisada: curva B.
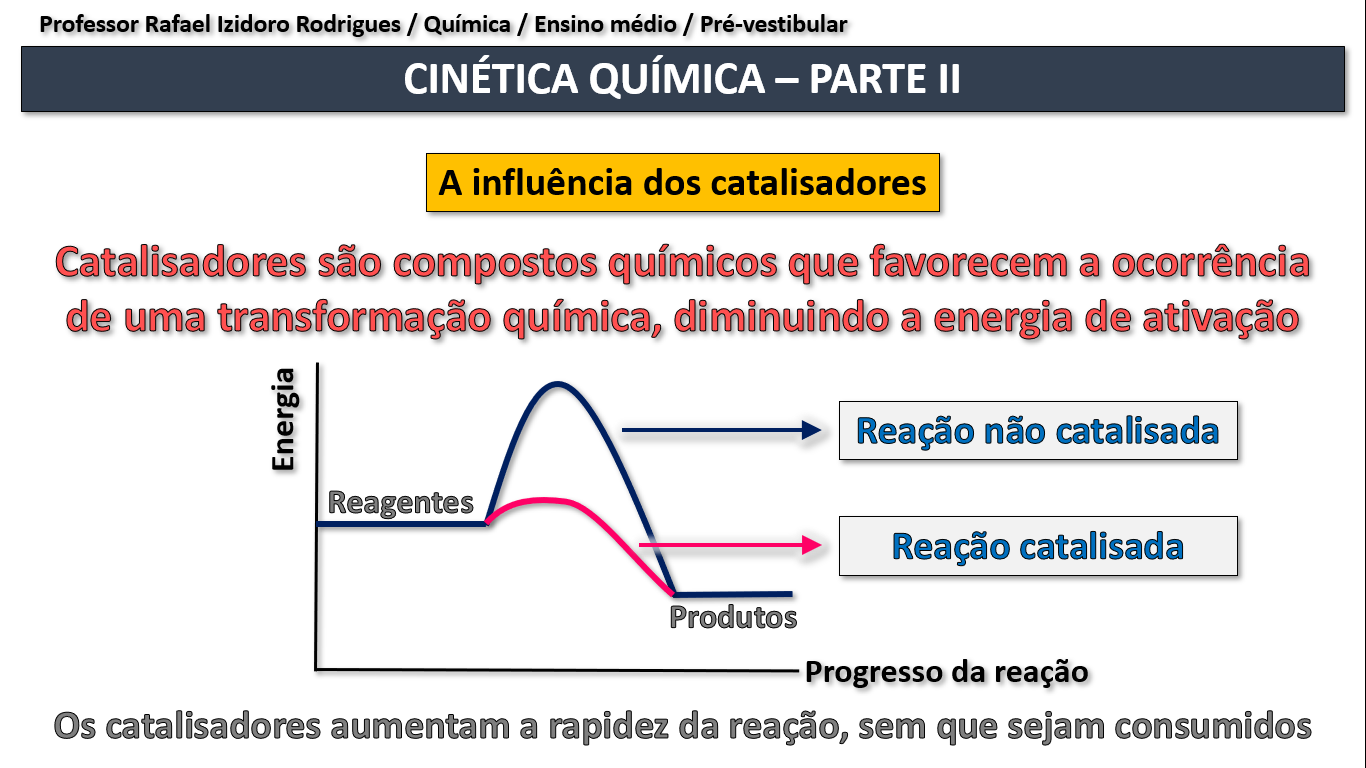
Quanto à energia de ativação.
EA = 70 kJ - 10 kJ = 60 kJ.
Quanto à variação de entalpia:
DH = 30 kJ - 10 kJ = 20 kJ.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.
Perguntas relacionadas
Materiais relacionados
 1 pág.
1 pág. 1 pág.
1 pág.




Compartilhar