(UERJ 2018) Um medicamento utilizado como laxante apresenta em sua composição química os sais
\(Na_2HPO_4\) e \(NaH_2PO_4\), nas concentrações de 142 g/L e 60 g/L, respectivamente. A eficácia do medicamento está relacionada à alta concentração salina, que provoca perda de água das células presentes no intestino.
Admitindo que cada um dos sais encontra-se 100% dissociado, calcule a concentração de íons Na+, em mol/L, no medicamento.
Em seguida, também em relação ao medicamento, nomeie o sal com menor concentração e a propriedade coligativa correspondente à sua ação laxante.
💡 2 Respostas
Estudante PD
Devemos determinart a concentração dos íons, separadamente, e posteriormente, totalizar.
Dissociação 1:
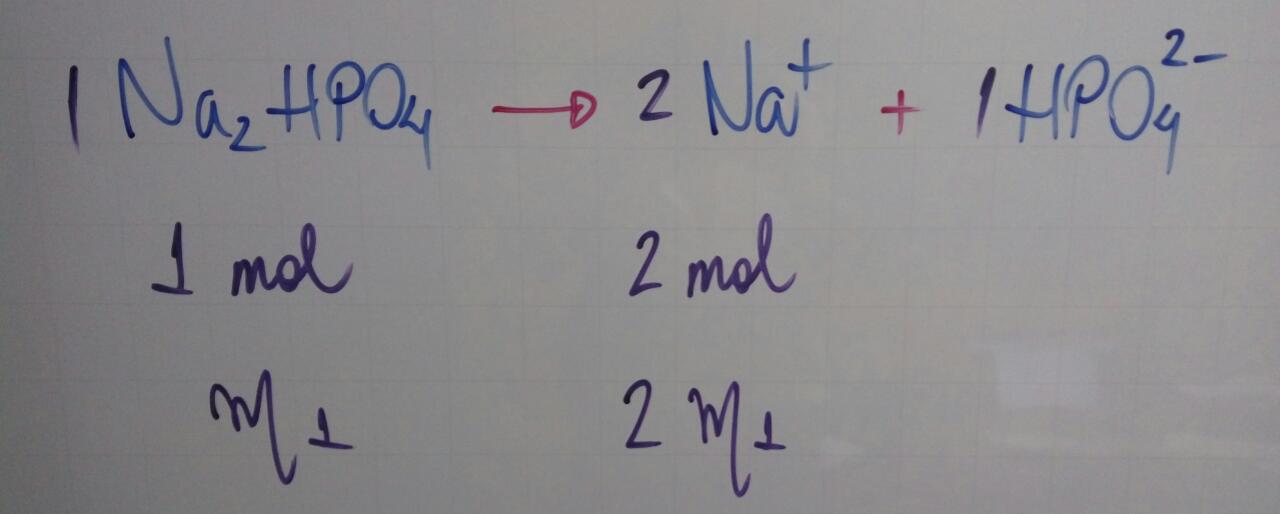
Dissociação 2:
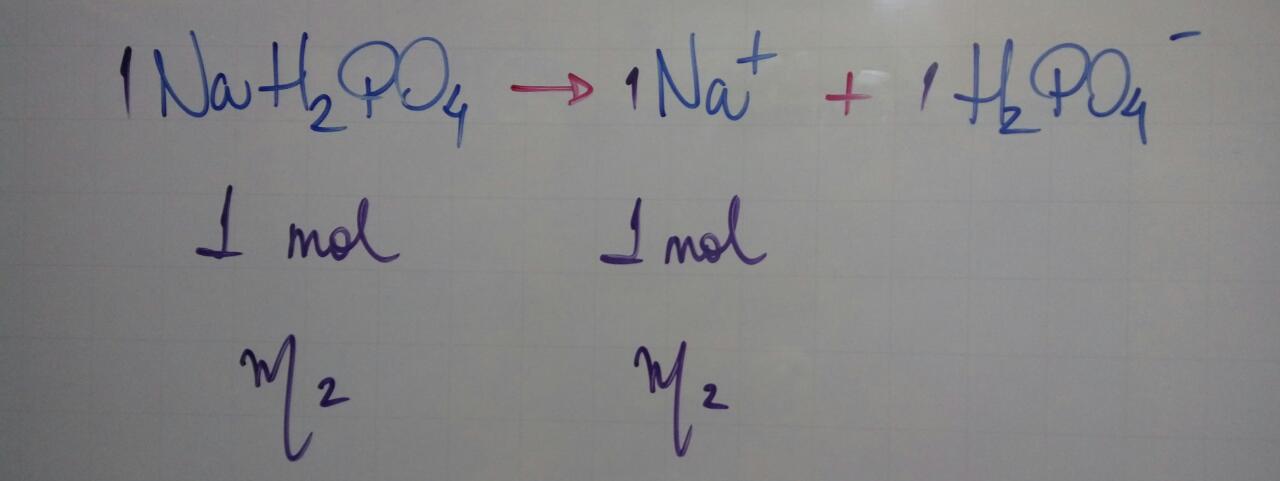
Arranjo matemático das fórmulas:
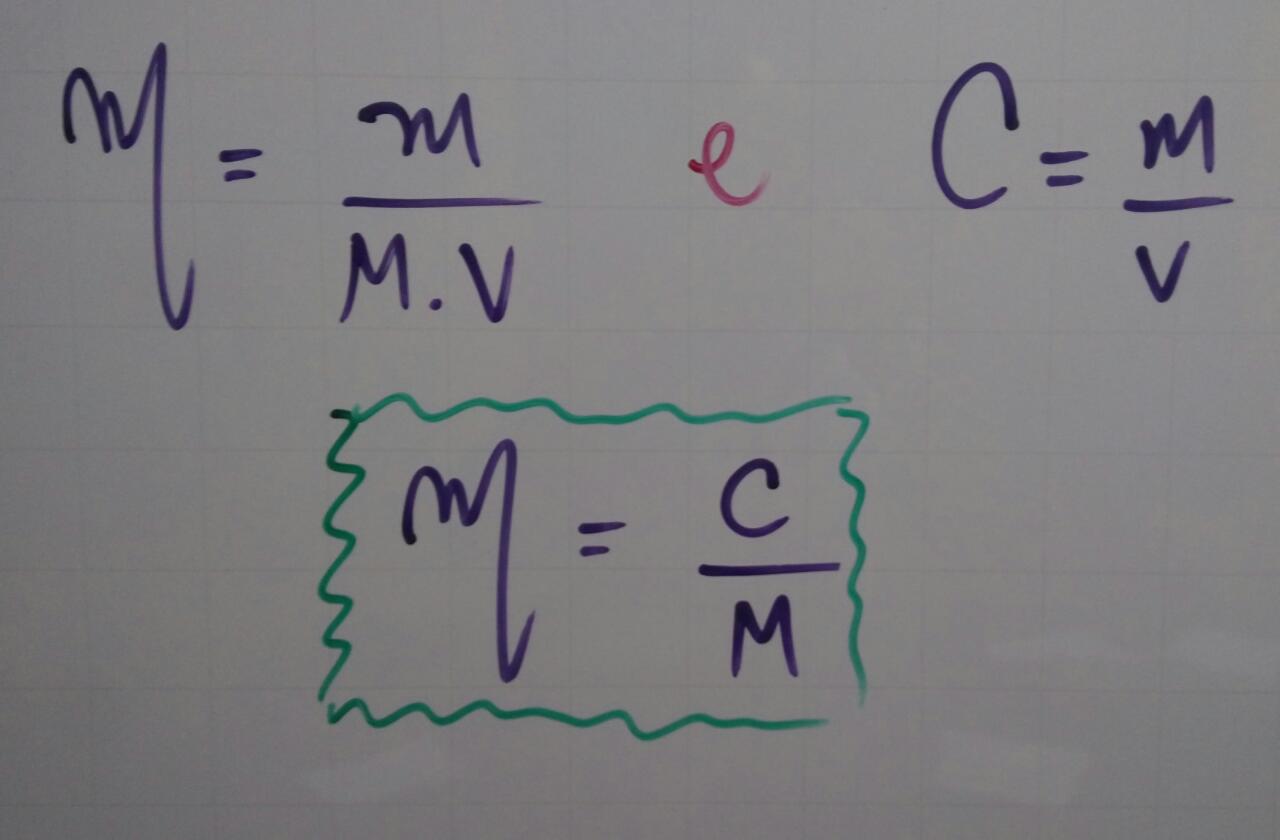
Após determinação das massas molares de cada sal:
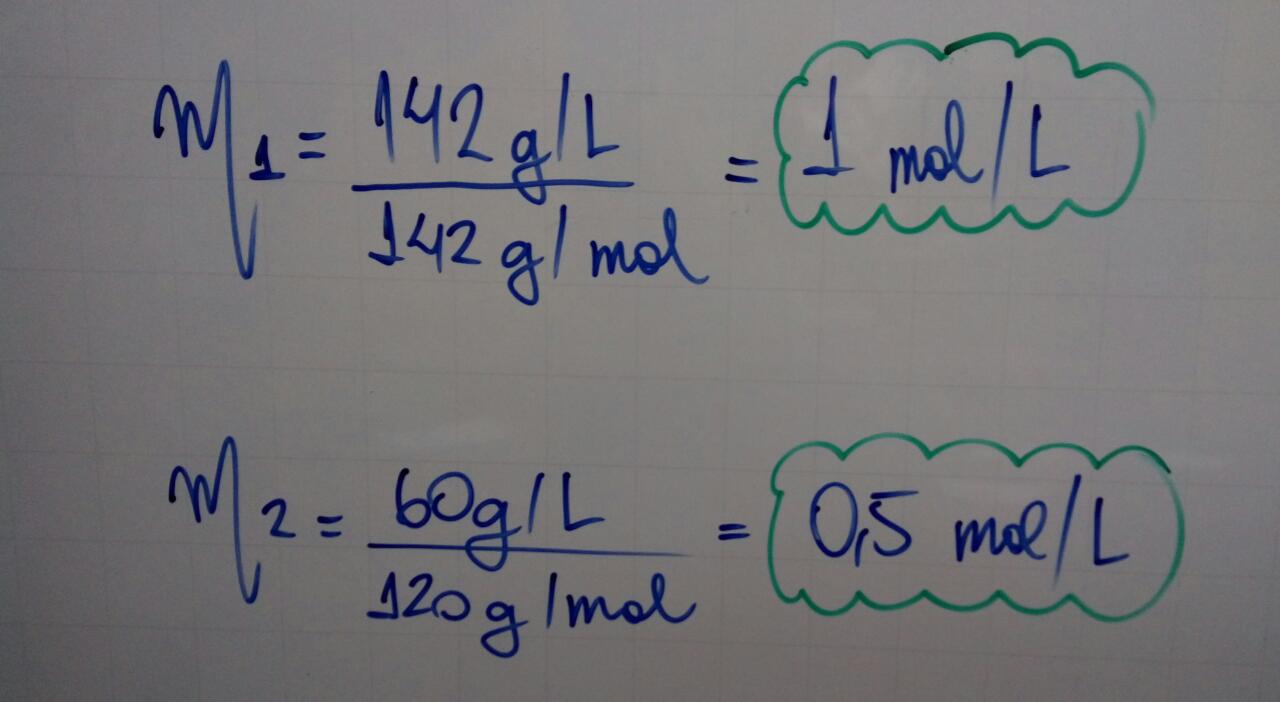
Cálculo da concentração de íons sódio (Na+):

Nome do sal de menor concentração:
Di-hidrogenofosfato de sódio.
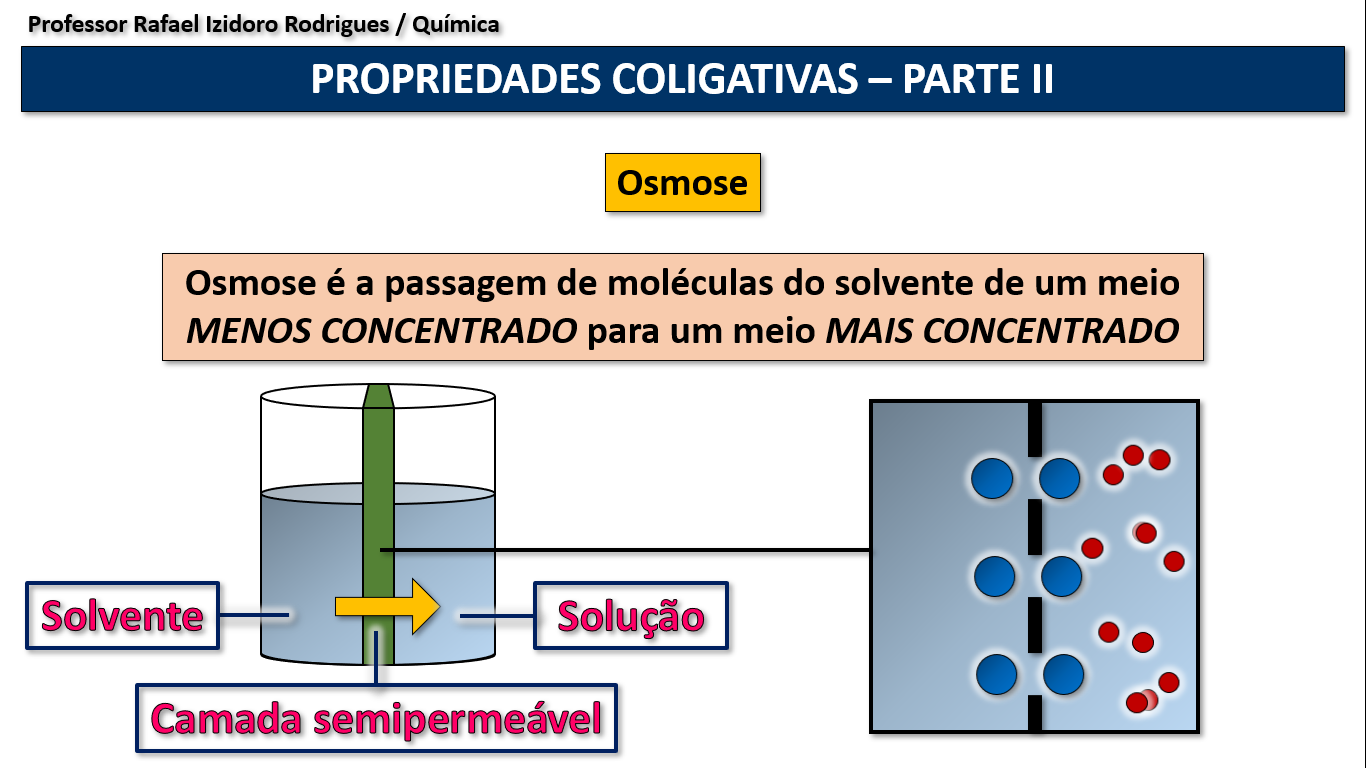
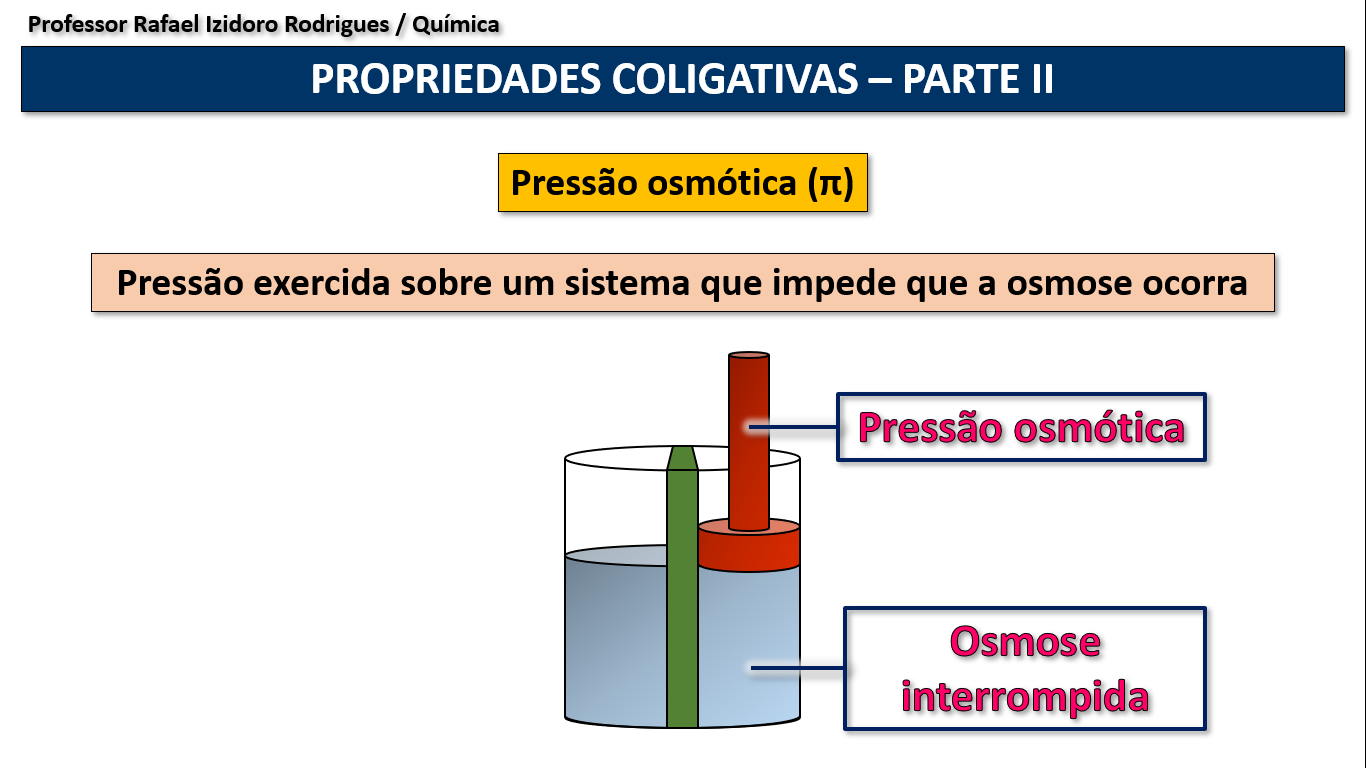
Propriedade coligativa: osmose.
Celso Bortoletto
Olá!
Primeiramente é necessário escrever as reações químicas de dissociação dos sais.
No medicamento, temos que a massa presente de é de 142 g/L. Sabendo que a massa molar do sal é de 142 g/mol, temos então que há 1 mol/L de .
Da mesma maneira, temos que a massa presente de texNaHPO4 é de 60 g/L. Sabendo que a massa molar do sal é de 120 g/mol, temos que há 0,5 mol/L de NaHPO4
Vemos pelas reações que 1 mol de gera 2 mols de íons e que 1 mol de gera 1 mol de íons .
Como temos 1 mol de , teremos após dissociação, 2 moles de íons e como há 0,5 mol de , teremos 0,5 mol de íons após dissociação.
Logo a concentração gerada de íons será de 2 + 0,5 = 2,5 mol/L.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 1 pág.
1 pág. 10 pág.
10 pág. 3 pág.
3 pág.




Compartilhar