ITA 2019 - Um dado indicador ácido-base tem constante de dissociação ácida igual a 3,0 x 10^−5.
A forma ácida desse indicador tem cor vermelha e sua forma básica tem cor azul. Com base nessas informações, assinale a opção que apresenta o valor aproximado da variação de pH para que ocorra a mudança de cor do
indicador de 75% da coloração vermelha para 75% da azul.
A ( ) 0,33 C ( ) 1,5 E ( ) 3,0
B ( ) 1,0 D ( ) 2,0
💡 2 Respostas
Camila Assis
Um indicador ácido-base (HIn) é um ácido fraco e apresenta o equilíbrio:
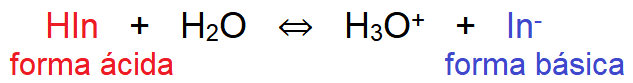
É dado o valor de k, que é igual a 3,0 x 10-5.
- Se temos 75% HIn: K = [H3O+] [In-] / [HIn]
Substituindo valores: 3,0 x 10-5 = [H3O+] . 0,25 / 0,75
[H3O+] = 9 x 10 -5 mol/L
pH = - log [H3O+] = - log 9 x 10 -5 ≈ 4,0
- Se temos 75% In-: K = [H3O+] [In-] / [HIn]
Substituindo valores: 3,0 x 10-5 = [H3O+] . 0,75 / 0,25
[H3O+] = 1 x 10 -5 mol/L
pH = - log [H3O+] = - log 1 x 10 -5 = 5,0
Podemos concluir que a variação de pH para que ocorra a mudança de cor é aproximadamente 1 (5,0 - 4,0 = 1,0)
Gabarito: letra B
Paulo Sousa
Letra "B"
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.
Perguntas relacionadas
1-O indicador HInd tem uma constante de dissociação ácida de 4,80x10-6 . A variação de absorbância de uma solução 8,00x10-5 mol L-1 de uma solução...
Qui310- Métodos Instrumentais de Análise Química
•UFJF
Kamylla Prata
Materiais relacionados
 12 pág.
12 pág.





Compartilhar