(UERJ 2015) Considere os seguintes valores das entalpias-padrão da síntese do HCl, a partir dos mesmos regentes no estado gasoso.
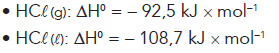
Calcule a entalpia-padrão, em kJ × mol\(^{-1}\), de vaporização do HCl e nomeie duas mudanças de estado físico dessa substância que sejam exotérmicas.
💡 3 Respostas
Battistelli
1) Primeiramente, devemos montar as equações de formação do ácido clorídrico gasoso e líquido, que corresponderão aos valores de ∆H0 fornecidos.
½ H2(g) + ½ Cl(g) → HCl(g) ∆H0 = − 92,5 kJ / mol
½ H2(g) + ½ Cl(g) → HCl(l) ∆H0 = − 108,7 kJ / mol
2) Como a questão nos pede a entalpia de vaporização, devemos inverter a equação do HCl líquido (junto com o ∆H0), de forma a somar as equações e termos a transição de estado físico do ácido clorídrico de líquido pra gasoso.
½ H2(g) + ½ Cl(g) → HCl(g) ∆H0 = − 92,5 kJ / mol
HCl(l) → ½ H2(g) + ½ Cl(g) ∆H0 = + 108,7 kJ / mol
Somando as equações:
HCl(l) → HCl(g) ∆H0 = 16,2 kJ / mol
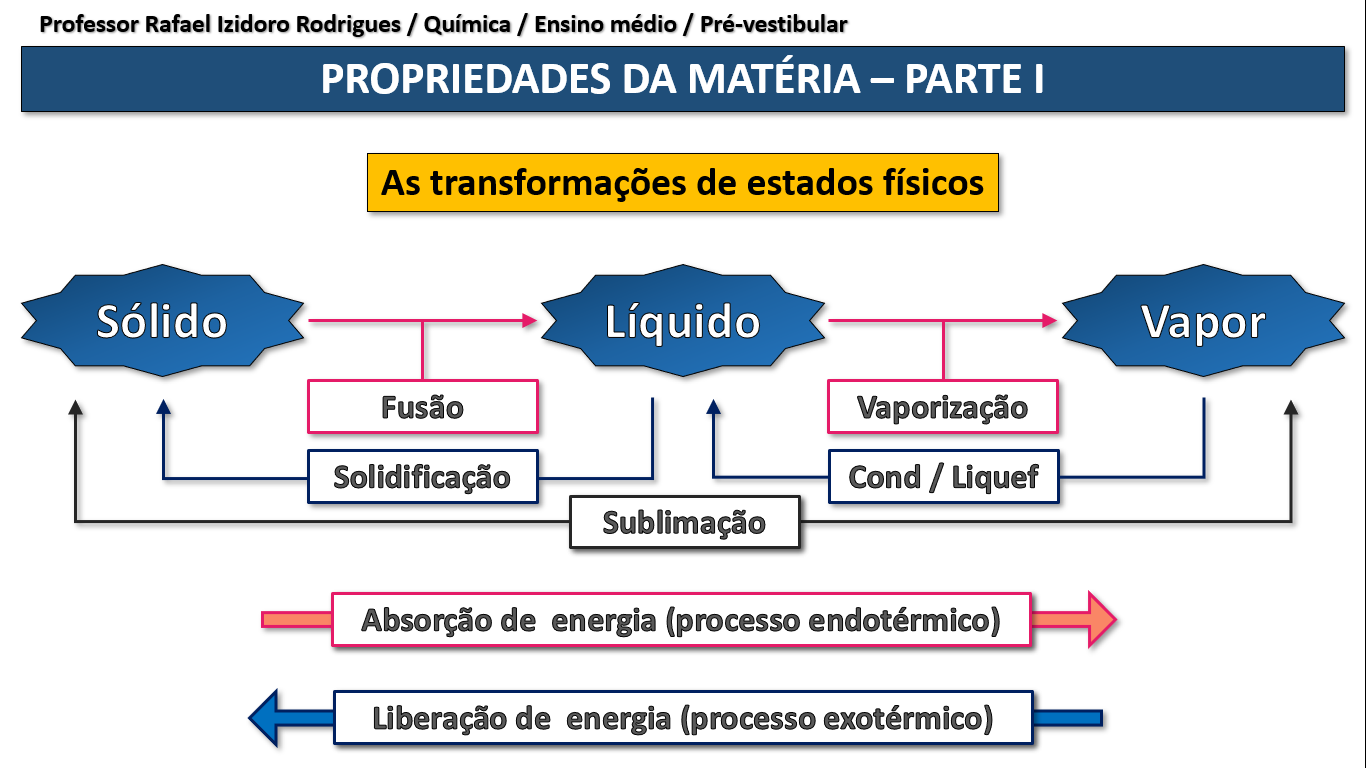
Como o ∆H0 é positivo, temos que a transição de estado físico do líquido para o gás é endotérmica, o que revela que a transição contrária é exotérmica, que é a condensação. Se a condensação é exotérmica, a solidificação também é, pois temos uma tendência de comportamento da molécula a produzir reações exotérmicas conforme mudamos o estado físico para uma situação onde as moléculas estão mais próximas.
Resposta
∆H0 vaporização = 16,2 kJ / mol
Solidificação e condensação são exotérmicos.
Estudante PD
Equação química da reação de vaporização do HCl:

Cálculo da entalpia de vaporização do HCl:


Transformações físicas exotérmicas:
Condensação e solidificação.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.
Perguntas relacionadas
Materiais relacionados
 1 pág.
1 pág.





Compartilhar