(ITA 2017) O diagrama de van Arkel-Ketelar apresenta uma visão integrada das ligações químicas de compostos binários,
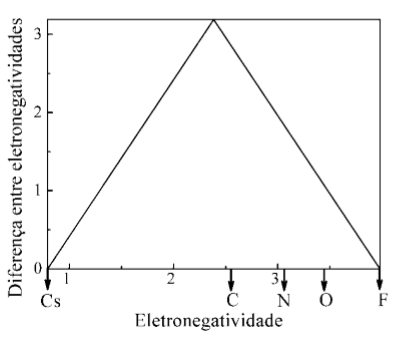
representando os três tipos clássicos de ligação nos vértices de um triângulo. Os vértices esquerdo e direito da base correspondem, respectivamente, aos elementos menos e mais eletronegativos, enquanto o vértice superior do triângulo representa o composto puramente iônico. Com base no diagrama, assinale a opção que apresenta o composto binário de maior caráter covalente.
A ( ) CCl4 B ( ) C3N4 C ( ) CO2 D ( ) NO E ( ) OF2
💡 7 Respostas
Camila Assis
O composto de maior caráter covalente será aquele onde teremos menor diferença de eletronegatividade entre os elementos, pois se há uma menor diferença entre a eletronegatividade de uma ligação entre átomos, a ligação é menos polarizada, daí possui maior caráter covalente.
Partindo daí teríamos o NO como resposta, pois possui a menor diferença de eletronegatividade, segundo o diagrama de van Arkel-Ketelar.
Porém, no diagrama, quanto mais próximo um composto estiver do vértice direito, maior será o caráter covalente da ligação química. Então, não basta apenas analisar o valor da diferença entre eletronegatividades, mas também o da eletronegatividade média do composto, daí temos o OF2 que se encaixa nas suposições, é o de maior caráter covalente.
Gabarito: letra E
Aryel Melo
Gabis Matos
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.







Compartilhar