(UERJ 2013) A equação química abaixo representa a reação da produção industrial de gás hidrogênio.
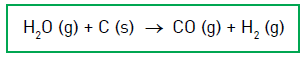
Na determinação da variação de entalpia dessa reação química, são consideradas as seguintes equações termoquímicas, a 25 °C e 1 atm:
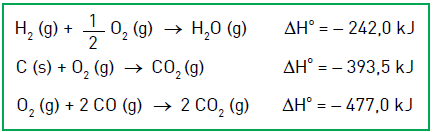
Calcule a energia, em quilojoules, necessária para a produção de 1 kg de gás hidrogênio e nomeie o agente redutor desse processo industrial.
💡 4 Respostas
Estudante PD
Lei de Hess
Vamos tentar ajeitar as equações de baixo para ficar igual à primeira
H2O ---- H2+ 1/2O2 H=242
C + O2 ----- CO2 H= -393,5
CO2 ----- CO + 1/2O2 H = 238,5
C+ H20 ---- H2 + CO H=87
1 g de H2 ------------87
1000g-----------------x
x=87000 KJ
Estudante PD
Através da lei de Hess:
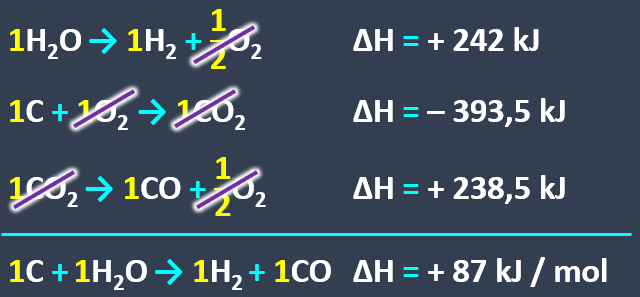
Para 1 kg de H2:
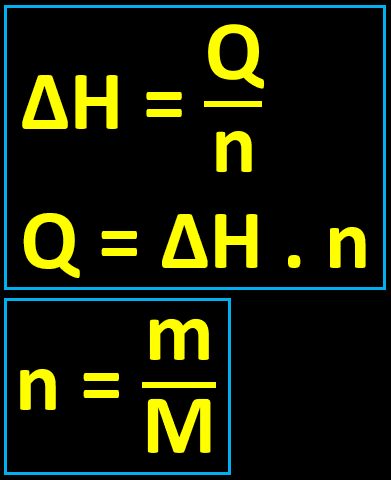
Ajustando as equações acima (1 kg = 1000 g e M(H2) = 2 g/mol):
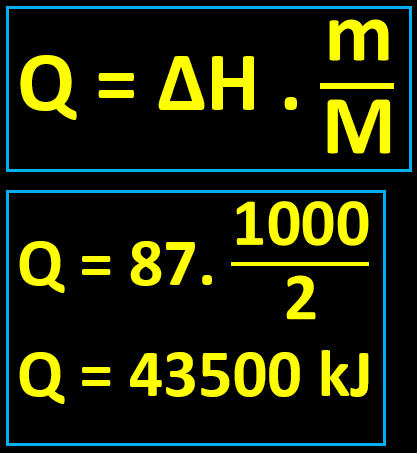
Quanto ao agente redutor:

Agente redutor: C.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.






Compartilhar