como resolver exercicio de quimica sobre "soluções ideais"
3) Uma solução líquida contém certa quantidade de tolueno e 1 mol de benzeno a 298 K. Nesta temperatura, a pressão de vapor do benzeno puro é de 75 Torr e do tolueno de 25 Torr. A pressão de vapor da mistura foi medida como 50 Torr. Admita a solução seja ideal, onde ambos líquidos seguem a lei de Raoult. Calcule a quantidade adicionada de tolueno e a fração molar de cada composto no líquido se esse sistema. (resp: 1 mol; xbz = xtl = 0,5)
💡 2 Respostas
Djenyffer Borges
ghbuhnknkjuuhuhuohojkplç~huuuu
Estudante PD
Seja:
n: número de mols de tolueno.
Xb: fração molar de benzeno.
Xt: fração molar do tolueno.
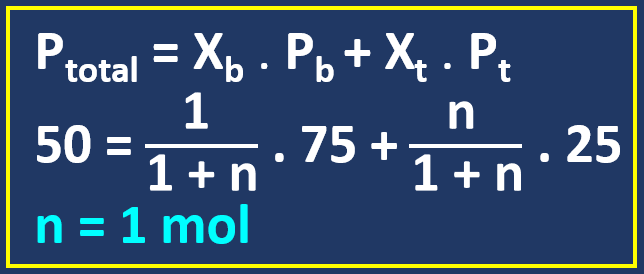
Frações molares:


✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.
Perguntas relacionadas
Materiais relacionados
 4 pág.
4 pág.




Compartilhar