As estruturas de Lewis são consequências da regra do octeto.
Ele utiliza os elétrons de valência de cada átomo para formar a estrutura, distribuindo os elétrons entre os átomos de forma a mostrar a conexão entre eles. Observe as estruturas de Lewis apresentadas a seguir, em que os pontos representam os elétrons de valência:
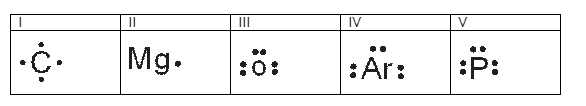
Fonte: elaborado pelo autro, 2019.
Estão corretamente representadas as seguintes estruturas:
|
( ) a) I e II |
||
|
( ) b) II e IV |
||
|
( ) c) I e III |
||
|
( ) d) III e IV |
||
|
( ) e) II e III. |
💡 5 Respostas
Junior Liberato
Letra C
Camila Assis
Temos os elétrons de valência (elétrons na última camada) para os átomos citados no enunciado:
C - 4 elétrons
Mg - 2 elétrons
O - 6 elétrons
Ar - 8 elétrons
P - 5 elétrons
Estão corretos: C e O
Gabarito: letra C
Jany Nunes
c- I e III
A partir da distribuição eletrônica dos compostos, podemos definir a quantidade de elétrons na camada de valência dos mesmos. Assim, temos:
C à
[He]2s22p2
Mg à
[Ne]3s2
O à
[He]2s22p4
Ar à[Ne]3s23p6
P à[Ne]3s23p3
Portanto, apenas o Carbono (C) e o Oxigênio (O) são apresentados corretamente, considerando a estrutura de Lewis.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta.
Perguntas relacionadas
Materiais relacionados
 1 pág.
1 pág. 18 pág.
18 pág.



Compartilhar