Questão 1 Recentemente, um artigo publicado em uma revista renomada relatou um caso de uma intoxicação fatal devido ao consumo de um derivado da tr...
Questão 1
Recentemente, um artigo publicado em uma revista renomada relatou um caso de uma intoxicação fatal devido ao consumo de um derivado da triptamina, conhecido como dipropiltriptamina (DPT). DPT é um composto alucinógeno reconhecido por induzir efeitos semelhantes aos da dimetiltriptamina (DMT, usado principalmente em rituais religiosos), porém com maior duração. No caso relatado, o individuo foi levado ao hospital para os devidos atendimentos. Amostras de soro (coletadas quatro horas após o consumo), sangue e urina foram analisadas com o auxílio de algumas técnicas da química analítica instrumental. Cromatogramas provindos de cromatografia gasosa (CG) indicaram a presença de DPT, contudo mais duas substâncias estavam presentes na amostra analisada (considerar os picos principais no cromatograma).
Fonte: NEUKAMM, M. A. et al. A fatal case of aspiration due to consumption of the hallucinogenic tryptamine derivative dipropyltryptamine (DPT). J Pharm Biomed Anal, [s. l.], v. 240, jan. 2024.
O cromatograma (fictício), Figura 1, simula a presença de três substâncias presentes na amostra de soro do paciente:
- DPT (dipropiltriptamina): 160 °C.
- Triptamine: 137 °C.
- DMT (dimetiltriptamina): 140 °C.
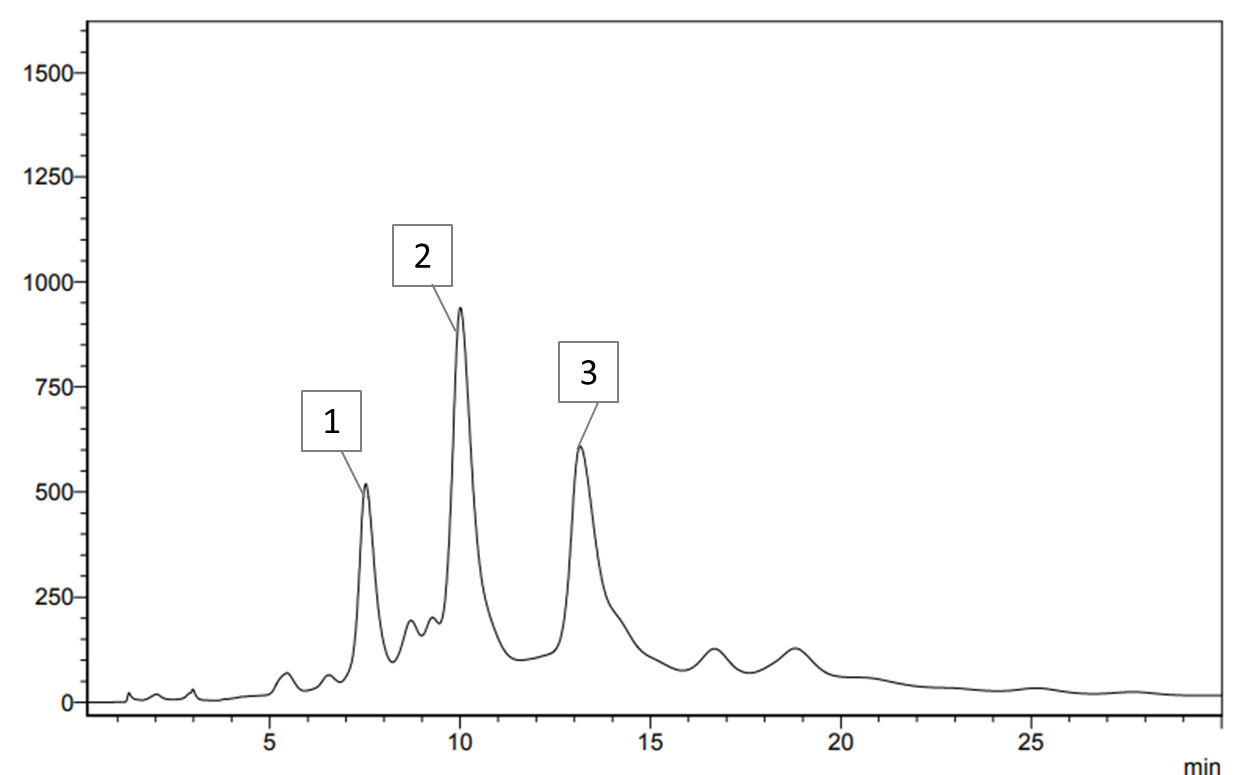
Figura 1 - Cromatograma de análise de soro do paciente com intoxicação
Fonte: a autora.
A partir das informações sobre métodos cromatográficos, bem como do ponto de ebulição de cada substancia, responda aos itens a seguir:
A) DESCREVA no mínimo três pontos-base do princípio da cromatografia gasosa.
B) RELACIONE os picos (1, 2 e 3) no cromatograma com cada uma das substâncias (DTP, triptamina, DMT). EXPLIQUE o motivo da ordem escolhida por você.
💡 3 Respostas
MD Engenharia
A cromatografia gasosa (CG) é uma técnica analítica utilizada para separar e identificar componentes de uma mistura volátil. A presença de dipropiltriptamina (DPT), triptamina e dimetiltriptamina (DMT) foi identificada no cromatograma, com pontos de fusão respectivos de 160 °C, 137 °C e 140 °C. A presença dessas substâncias foi confirmada através de técnicas de cromatografia gasosa (CG). No entanto, o paciente faleceu devido à aspiração após o consumo de DPT.
- O artigo relata um caso de intoxicação fatal devido ao consumo de dipropiltriptamina (DPT), um alucinógeno semelhante à dimetiltriptamina (DMT).
- Cromatogramas provenientes de cromatografia gasosa (CG) indicaram a presença de DPT, triptamina e DMT na amostra analisada, com pontos de fusão respectivos de 160 °C, 137 °C e 140 °C.
- O paciente foi levado ao hospital, mas faleceu devido à aspiração após o consumo de DPT, conforme indicado pelo relatório.
- A análise forense das amostras de soro, sangue e urina foi fundamental para determinar as substâncias presentes e ajudar na investigação do caso.
#SPJ1
MD Engenharia
A) Os três pontos-base do princípio da cromatografia gasosa são: 1) Separação dos componentes de uma mistura através da interação entre a fase móvel (gás) e a fase estacionária (coluna cromatográfica); 2) Os componentes da amostra se distribuem entre a fase móvel e estacionária, resultando em diferentes tempos de retenção; 3) A detecção dos componentes é feita através da análise dos tempos de retenção e das áreas dos picos no cromatograma.
B) No cromatograma, o pico 1 corresponde à dipropiltriptamina (DPT), o pico 2 à triptamina e o pico 3 à dimetiltriptamina (DMT). A ordem é determinada pelos pontos de ebulição: DPT (160 °C), DMT (140 °C) e triptamina (137 °C). Portanto, a substância com o ponto de ebulição mais alto aparece primeiro, seguida pelas de menor ponto de ebulição.
Na cromatografia gasosa, os picos são eluídos da coluna cromatográfica com base em sua interação com a fase móvel e estacionária, resultando em diferentes tempos de retenção. Assim, as substâncias são detectadas e identificadas com base em seus tempos de retenção e características físico-químicas.
João Antonio Marchezan Dantas
A) Os três pontos-base do princípio da cromatografia gasosa são: 1) Separação dos componentes de uma mistura através da interação entre a fase móvel (gás) e a fase estacionária (coluna cromatográfica); 2) Os componentes da amostra se distribuem entre a fase móvel e estacionária, resultando em diferentes tempos de retenção; 3) A detecção dos componentes é feita através da análise dos tempos de retenção e das áreas dos picos no cromatograma.
B) No cromatograma, o pico 1 corresponde à dipropiltriptamina (DPT), o pico 2 à triptamina e o pico 3 à dimetiltriptamina (DMT). A ordem é determinada pelos pontos de ebulição: DPT (160 °C), DMT (140 °C) e triptamina (137 °C). Portanto, a substância com o ponto de ebulição mais alto aparece primeiro, seguida pelas de menor ponto de ebulição.
Na cromatografia gasosa, os picos são eluídos da coluna cromatográfica com base em sua interação com a fase móvel e estacionária, resultando em diferentes tempos de retenção. Assim, as substâncias são detectadas e identificadas com base em seus tempos de retenção e características físico-químicas.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
A DPT é reconhecida por induzir efeitos semelhantes aos da dimetiltriptamina (DMT), porém com uma duração maior. A ingestão excessiva de DPT provav...
Química Analítica Instrumental
•UniCesumar
lenise valente
O cromatograma (fictício), Figura 1, simula a presença de três substâncias presentes na amostra de soro do paciente: - DPT (dipropiltriptamina):...
Química Analítica Instrumental
•UNICESUMAR
hercules viana
Materiais relacionados
 2 pág.
2 pág. 2 pág.
2 pág. 2 pág.
2 pág.




Compartilhar