balanceamento
Indique três maneiras de se aumentar a concentração de NH3 no equilíbrio para a seguinte reação: N2(g) + 3H2(g) 2NH3(g) + 22 kcal Justifique cada resposta.
💡 2 Respostas
Rodrigo Lenz
° possibilidade: Se aumentar a concentração de N2, o equilíbrio se deslocará para a direção do NH3. 2° possibilidade: Se aumentar a concentração de H2, o equilíbrio se deslocará para direção do NH3. 3° possibilidade: Como a reação é endotérmica, se aumentar a temperatura o +22kcal irá absorver essa temperatura, entrando em equilíbrio químico.
Especialistas PD
Para aumentarmos a concentração do produto, NH3, nesta reação: N2(g) + 3H2(g) ⇔ 2NH3(g) + 22 kcal, temos que deslocar o equilíbrio químico para o sentido dos produtos!
Segundo o Princípio de Le Chatelier, quando se aplica uma força em um sistema em equilíbrio, ele tende a se reajustar no sentido de diminuir os efeitos dessa força.
- Então se aumentarmos a concentração dos reagentes, o equilíbrio se deslocará para o sentido direto.
- O aumento da pressão total desloca o equilíbrio no sentido do menor volume, que neste caso, é o sentido direto.
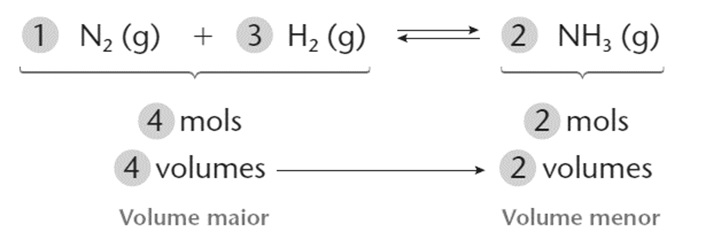
- Esta reação libera calor (+ 22 kcal), é uma reação exotérmica. A diminuição da temperatura desloca o equilíbrio no sentido da reação exotérmica, que neste caso é o sentido direto.

✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta







Compartilhar