Determine a composição, em porcentagem atômica, de uma liga que consiste em 97%p em alumínio e 3%p em cobre.
💡 5 Respostas
Julio C. Lourenço
Olá!
Considere os pesos atômicos do cobre e do alumínio:
Cobre - 63,54 g/mol
Alumínio - 26,98 g/mol
Aqui eu irei fazer sem usar a fórmula, apenas de forma lógica. Acho que fica mais fácil para ser gravado, caso você esqueça da fórmula! Vamos lá!
Em 100 g da liga, 97 g são alumínio e 3 g são cobre. Vamos fazer uma regra de 3 para saber quantos mols temos ao total:
----
63,54 g Cu - 1 mol
3 g - X mols
X = 0,0472 mols de Cu
26,98 g de Al - 1 mol
97 g - Y mols
Y = 3,5952 mols de Al
----
O total de mols será: 3,5952 + 0,0472 = 3,6424 mols
Observe que a % atômica é a mesma que a % em mols, pois o número de mols basta multiplicar pelo número de avogrado. Então, a % de cada elemento em atômico será:
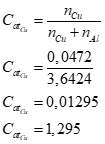
E a % at. de Al será:
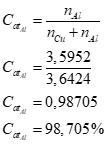
Resposta: aproximada 1,3 % Cu - 98,7 % Al.
Bons estudos!
Felipe Franco
Cl' = (5%) do cobre
C2' = (95%) da Plantina
Cobre - Cl' = A1 => 63,55 g/mol
Platina - A² = 195,8 g/mol
CL' = [ (Cl * A2) / (Cl * A2) + (C2 * A1) ] * 100
A= Peso atômico
C = porcentagem do peso do material
Cl' = [ ( 5* 195,8 g/mol) / ( 5* 195,8) + (95 * 63,55 g/mol)] * 100
Cl' = 13,95% g/mol do cobre
C2' = [ (c2 * a1) / (cl * A2) + (c2 * A1)] * 100
C2' = [ (95 * 63,55 g/mol) / (5 * 195,8 g/mol) + (95 * 63,55 g/mol)
C2' = 86,05 % g/mol .
CL + C2 = 100%
ta aê pô :)
Felipe Franco
precisar grita aê.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Qual é a composição, em porcentagem atômica, de uma liga que consiste em 97%p Fe e 3%p Si/
Fundamentos de Ciências dos Materiais
•UDESC
Brenda Verch
Qual é a composição, em porcentagem atômica, de uma liga que contém 98 g de estanho e 65 g de chumbo?
Ciência dos Materiais
•PITÁGORAS
Douglas Soares
Materiais relacionados
 1 pág.
1 pág.




Compartilhar