explique energia de ionização, da tabela periodica
Respostas
Debora Cristina
há 11 anos
Se considerarmos os elementos em uma mesma família ou num mesmo período da tabela periódica, veremos que conforme aumentam os números atômicos, menores são as energias de ionização( energia mínima necessária para retirar um elétron), porque mais afastados do núcleo os elétrons estão. Desse modo, a energia de ionização cresce na tabela periódica de baixo para cima e da esquerda para a direita. Portanto, a energia de ionização é uma propriedade periódica.

Libere essa resposta sem enrolação!


Cadastre-se ou realize login
Ao continuar, você aceita os Termos de Uso e Política de Privacidade


Especialistas PD
há 7 anos
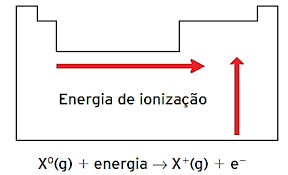
Energia de Ionização, também denominada de Potencial de ionização, corresponde à energia mínima necessária para retirar um elétron de um átomo ou íon no estado gasoso.
Na prática, o mais importante é primeiro potencial de ionização ou primeira energia de ionização, que corresponde à remoção do primeiro elétron. Ela costuma ser a menor energia de ionização, pois como esse elétron é o mais afastado do núcleo, a sua força de atração com o núcleo é a menor, precisando de menos energia e sendo mais fácil removê-lo.
Além disso, com a perda de elétrons, o raio atômico diminui e o íon fica cada vez mais positivo, portanto, a atração com o núcleo fica mais forte e, consequentemente, será necessária mais energia para retirar o próximo elétron e assim sucessivamente.
Estudante PD
há 4 anos
A minima energia necessaria para remover um elétron de um átomo isolado , no seu estado fundamental , está diretamente ligado ao fato de o núcleo exercer uma força de atração sobre os elétrons .





