qual a lei dos gases reais?
💡 3 Respostas
Caio Menezes
Os gases reais, para pressões não muito baixas e temperaturas não muito altas, têm comportamento que se desvia do comportamento ideal. A mais conhecida equação de estado para gases reais é a equação de Van der Waals:
{P+ [a.(n^2)/(V^2)]}.[V-(n.b)] = n.R.T
Onde:
P = pressão dos gás ideal
V = Volume do gás ideal
n = número de moles
R = Constante Universal dos gases perfeitos
T = Temperatura
a e b são constantes de Van der Waals, determinadas pela natureza do gás na finalidade de que ocorra a maior congruência possível entre a equação dos gases reais e o comportamento observado em experimentos.
A constante a de Van der Waals está associada às forças intermoleculares de atração e quanto mais alto o seu valor, maiores são os módulos destas forças. Como a energia interna está diretamente relacionada à temperatura, quanto maiores os módulos das forças intermoleculares mais altos são os pontos de fusão e de ebulição da substância em questão. Assim, por exemplo, um valor alto para a constante a de Van der Waals pode significar um alto ponto de ebulição.
A constante b é o covolume, ou seja, o volume excluído por mol de moléculas. Ela está associada às forças intermoleculares de repulsão, que se tornam importantes quando as moléculas estão muito próximas umas das outras. Estas forças determinam o grau de dificuldade na compressão de uma substância nas fases de líquido ou de sólido. Indiretamente, as forças intermoleculares de repulsão determinam também o tamanho próprio das moléculas de um gás.
Fontes:
* Wikipedia
* http://coral.ufsm.br/gef/Calor/calor11.pdf
Flávio Sousa
modelo de van der waals
RT = (P+a/v²)x(V-b)
Onde o a/v² é o aumento da pressão considerando o volume das moléculas do gás
e b é a diminuição do volume considerando as interações entermoleculares das moléculas do gás.
Especialistas PD
Uma das equações que descreve os gases reais é a equação de van der Walls que considera uma correção na pressão e no volume do gás. Van der Waals introduziu a constante a, para correção da pressão e a constante b para correção do volume do gás real.
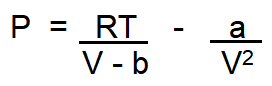
Onde a e b são específicos para cada substância;
a: representa as forças de atração entre as moléculas;
b: representa o volume das moléculas (co-volume)
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Compartilhar