UERJ 2012 - Em uma das etapas do ciclo de Krebs, ocorre uma reação química na qual o íon succinato é consumido.
Observe a fórmula estrutural desse íon:
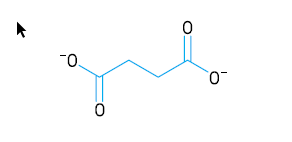
Na reação de consumo, o succinato perde dois átomos de hidrogênio, formando o íon fumarato.
Sabendo que o íon fumarato é um isômero geométrico trans, sua fórmula estrutural corresponde a:
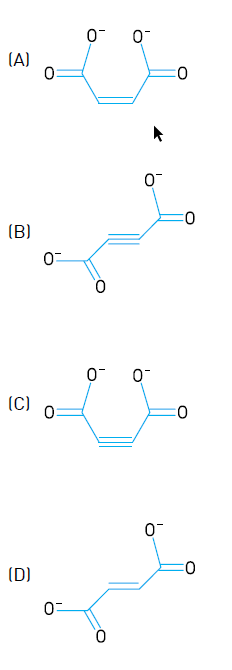
💡 1 Resposta
Camila Assis
Na formação do íon fumarato temos a eliminação de dois hidrogênios, havendo então, a formação de uma ligação dupla. A isomeria cis-trans (ou isomeria geométrica) é um tipo de estereoisomeria dos alcenos e cicloalcanos. No isómero cis, os substituintes estão no mesmo lado da dupla ligação ou no mesmo lado do cicloalcano; no isômero trans, os substituintes estão no lado oposto da dupla ligação ou em lados opostos do cicloalcano. Então o isômero trans está na alternativa D, onde temos cada substituinte em lados opostos da dupla ligação.
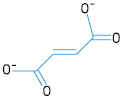
Gabarito: letra D
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta






Compartilhar