(IME 2018) Considere as reações abaixo:
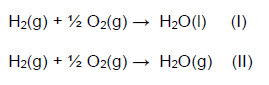
Assinale a alternativa correta.
(A) O decréscimo de entropia é menor na reação (I) do que na reação (II).
(B) O acréscimo de entropia na reação (I) é maior do que na reação (II).
(C) O decréscimo de entropia é menor na reação (II) do que na reação (I).
(D) O acréscimo de entropia na reação (II) é maior do que na reação (I).
(E) A variação de entropia é igual em ambas as reações.
💡 1 Resposta
Estudante PD
Em ambos os casos haverá decréscimo de entropia, já que o número de mols nos produtos é menor que o número de mols nos reagentes.
Reação I: o produto se encontra do estado LÍQUIDO
Reação II: o produto se encontra no estado GASOSO.
No estado gasoso a desordem é maior (maior entropia).
No estado líquido a desordem é menor (menor entropia).
É necessário que haja maior descréscimo de entropia para que se atinja um maior grau de organização.
Alternativa C.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 1 pág.
1 pág.






Compartilhar