(UERJ 2014) A reação química entre o gás hidrogênio e o monóxido de nitrogênio, representada a seguir, foi analisada em duas séries de experimentos.
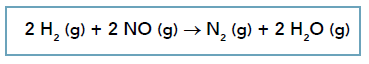
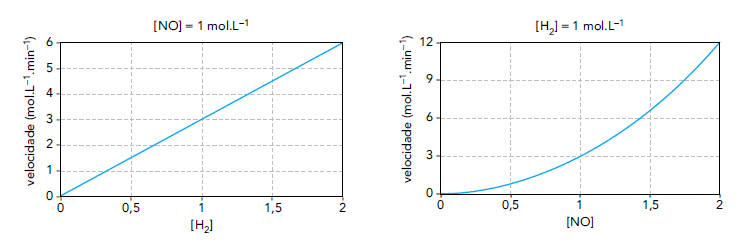
Na primeira série, a velocidade de reação foi medida em função da concentração de hidrogênio, mantendo-se a concentração de monóxido de nitrogênio constante em 1 mol.L\(^{-1}\) . Na segunda série, determinou-se a velocidade em função da concentração de monóxido de nitrogênio, mantendo-se a concentração de hidrogênio constante em 1 mol.L\(^{-1}\). Os resultados dos experimentos estão apresentados nos gráficos.
Determine a ordem de reação de cada um dos reagentes e calcule o valor da constante cinética.
💡 3 Respostas
Estudante PD
Seja, algébricamente, a equação de velocidade:

Para o gráfico da primeira série, escolhendo as concentrações 1 e 2 para o H2, teremos duas equações.
Dividindo uma equação pela outra, determinamos x:
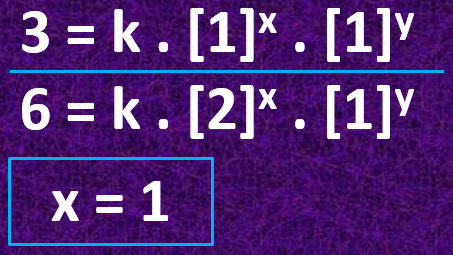
Para o gráfico da segunda série, escolhendo as concentrações 1 e 2 para o NO, teremos duas equações.
Dividindo uma equação pela outra, determinamos y:
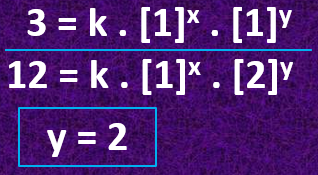
Para a ordem da reação, devemos somar x + y:
x + y = 1 + 2 = 3
Para a constante k, podemos usar:
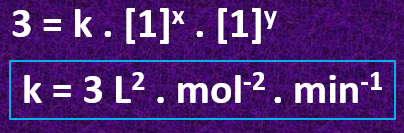
Rhaulen Mello
A velocidade de uma reação química é calculada a partir das concentrações dos reagentes. Para a reação em questão, a velocidade é dada por:
v = k · [H2]x · [NO]y
Onde:
v = velocidade da reação
k = constante cinética da reação
x = ordem de reação para o H2
y = ordem de reação para o NO
A ordem de reação para o hidrogênio é determinada a partir dos resultados do experimento com concentração fixa de monóxido de nitrogênio.
Assim, podem-se escolher dois pontos do primeiro gráfico:
• [H2] = 1 mol · L–1 e v = 3 mol · L–1 · min–1
• [H2] = 2 mol · L–1 e v = 6 mol · L–1 · min–1
Nota-se que, quando a concentração de H2 duplica de 1 mol · L–1 para 2 mol · L–1 a velocidade também duplica de 3 mol · L–1 · min–1 para 6 mol · L–1 · min–1.
Deduz-se, portanto, que x = 1. Logo, a ordem de reação para o hidrogênio é igual a 1.
A ordem de reação para o monóxido de nitrogênio é determinada a partir dos resultados do experimento com concentração fixa de hidrogênio.
Assim, podem-se escolher dois pontos do segundo gráfico:
• [NO] = 1 mol · L–1 e v = 3 mol · L–1 · min–1
• [NO] = 2 mol · L–1 e v = 12 mol · L–1 · min–1
Nota-se que, quando a concentração de NO duplica de 1 mol · L–1 para 2 mol · L–1 , a velocidade quadruplica de 3 mol · L–1 · min–1 para 12 mol · L–1 · min–1.
Deduz-se, portanto, que y = 2. Logo, a ordem de reação para o monóxido de nitrogênio é igual a 2.
Com base nesses resultados, a expressão de velocidade desta reação corresponde a:
v = k · [H2]1 · [NO]2
A constante cinética k da reação é determinada pela substituição dos valores obtidos em um dos experimentos.
Optando-se pelo experimento no qual [H2] = [NO] = 1 mol · L–1, a velocidade é igual a 3 mol · L–1 · min–1.
Substituindo-se os valores na equação:
3 = k · 1 · 12
k = 3 L2 · mol–2 · min–1
Thiago Barros
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta




Compartilhar