" Uma teoria de distribuição dos elétrons foi proposta por Linus Pauling (...)
(...) resultando num diagrama que apresenta sobre os níveis de energia propostos por Niels Bohr uma seqüência ordenada de distribuição segundo uma ordem crescente de energia dos elétrons.”
Utilizando o diagrama de Linus Pauling, apresente a distribuição eletrônica do átomo de cobre Cu. Em seguida, apresente também a distribuição do íon Cu2+.
💡 9 Respostas
Camila Assis
Utilizando o diagrama de Linus Pauling, TEORICAMENTE temos:
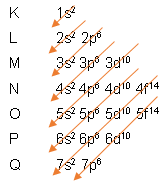
29Cu: 1s2 2s2 2p6 3s2 3p6 4s2 3d9
para o íons Cu2+, onde o cobre perde 2 elétrons na sua camada de valência (4ª camada), temos:
29Cu2+: 1s2 2s2 2p6 3s2 3p6 3d9
ATENÇÃO:
O elemento cobre é uma das exceções na distribuição de Linus Pauling, assim como o cromo, o ouro e a prata, devido por questão de estabilização de elétrons em camadas, essa distribuição eletrônica seria antiquada, pois, o subnível d possui 5 orbitais, que são os orbitais a serem preenchidas por dois elétrons em cada orbital para que o cobre fique estabilizado, deveriam ter dez elétrons ocupando os orbitais, ou seja, dois elétrons para cada orbital, não sendo possível o preenchimento neles com um orbital incompleto.
Então, para que adquira a estabilidade, devemos migrar um elétron de [4s2], ficando [4s1] para o [3d9] ficando [3d10], assim teremos a seguinte distribuição eletrônica experimental do cobre (Z = 29):
29Cu: 1s2 2s2 2p6 3s2 3p6 4s1 3d10
29Cu2+: 1s2 2s2 2p6 3s2 3p6 3d9
Yasha Gonçalves
Cu+2 (retirar dois elétrons da camada de valência mais distante do núcleo, no caso seria a N que corresponde ao 4s1 e M que corresponde a 3d10, que passa a ser 3d9) = 1s2 2s2 2p6 3s2 3p6 3d9
Adriano Malheiros
Obrigado Camila assis e Yasha. RESPOSTA CORRETA !
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 1 pág.
1 pág.



Compartilhar