1. Explique como varia a solubilidade dos halogênios?
💡 2 Respostas
Guilherme Lima
O estado de agregação desses elementos é variado, sendo o Flúor e o Cloro gasosos, o Bromo líquido e, o Iodo e o Astato sólidos. Todos, a exceção do Astato, possuem atomicidade 2, ou seja, na natureza encontra-se (mesmo que dificilmente, devido a alta reatividade dos halogênios) 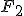 (gás flúor) e não F,
(gás flúor) e não F,  (sólido Iodo) e não I: apenas o Astato é monoatômico (At). A explicação dessa diversidade de estados físicos para um mesmo tipo de elementos está na densidade eletrônica de cada um: quanto maior o número atômico maiores as forças intermoleculares, sendo assim, explica-se o porquê de o Flúor (Z = 9) ser gasoso e o Iodo (Z = 53) ser sólido.
(sólido Iodo) e não I: apenas o Astato é monoatômico (At). A explicação dessa diversidade de estados físicos para um mesmo tipo de elementos está na densidade eletrônica de cada um: quanto maior o número atômico maiores as forças intermoleculares, sendo assim, explica-se o porquê de o Flúor (Z = 9) ser gasoso e o Iodo (Z = 53) ser sólido.
Outra explicação, junto ao aumento de densidade eletrônica, é a densidade específica e os pontos de fusão e ebulição.
Como são substâncias apolares, são pouco solúveis em meio aquoso.
Camila Assis
As forças existentes entre essas moléculas tornam-se mais intensas, com o aumento do número atômico do halogênio, o que justifica o crescimento dos pontos de fusão e ebulição dessas substâncias, indo do flúor para o iodo, à temperatura ambiente, o flúor e cloro são gases, o bromo é líquido e o iodo é um sólido. Todos, a exceção do Astato, possuem atomicidade 2, ou seja, na natureza encontra-se (mesmo que dificilmente, devido a alta reatividade dos halogênios) F2 (gás flúor) e I2 (sólido). A explicação dessa diversidade de estados físicos para um mesmo tipo de elementos está na densidade eletrônica de cada um: quanto maior o número atômico maiores as forças intermoleculares, sendo assim, explica-se o porquê de o Flúor (Z = 9) ser gasoso e o Iodo (Z = 53) ser sólido. Outra explicação, junto ao aumento de densidade eletrônica, é a densidade específica e os pontos de fusão e ebulição. Como são substâncias apolares, são pouco solúveis em meio aquoso.
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta
Perguntas relacionadas
Materiais relacionados
 4 pág.
4 pág. 2 pág.
2 pág.




Compartilhar