Me ajudem nesta questão ? Agradeço muito !! Determine o número de prótons, elétrons e nêutrons em casa átomo:
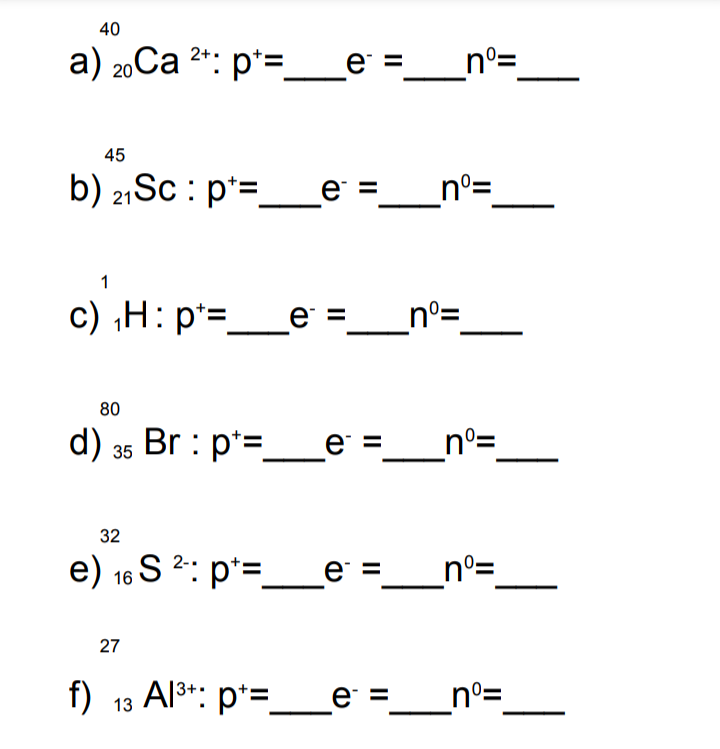
💡 1 Resposta
Fernanda Franco
Os números na parte de baixo do elemento é o número atômico (Z), que é igual ao número de prótons.
Vale lembrar, também, que a massa atômica é dada pela soma do número de prótons mais o número de nêutrons (n):
A = Z + n
Ou
n = A -Z
O número de elétrons é igual ao número de prótons, porém quando há um íon (cations ou anions), esses números se diferem. Para cations, que possuem carga positiva, se subtrai o número de elétrons de acordo com o número de carga. Para anions, se soma o numero de eletrons de acordo com o número de carga.
a) Ca: A=40; Z=20 (A é o número superior e Z é o número inferior).
Conforme explicado anteriormente:
Z = p+ = 20
e- = 20 - 2 =18 (se subtrai 2 por conta da carga +2)
n = A - Z = 40-20 = 20
p+ = 20; e- = 18; n =20
b) Sc: p+ = 21; e- 21 (não é um íon); n = 24
c) H: p+ = 1; e- =1; n=0
d) Br: p+ = 35; e- = 35; n= 45
e) S: p+ = 16; e- = 18; n=16
f) Al: p+ = 13; e- = 10; n= 14
✏️ Responder
Para escrever sua resposta aqui, entre ou crie uma conta




Compartilhar