73br- Ligação Metálica, Coesão do Retículo Cristalino, Volume Ocupado da Cela Unitária
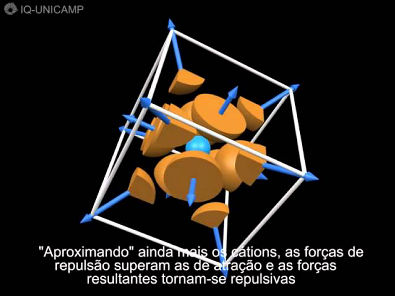

Ligação Metálica, Coesão do Retículo Cristalino, Volume Ocupado da Cela Unitária Maximização da coesão do retículo cristalino Maximização do volume ocupado das celas unitárias O deslocamento dos cátions não tem significado físico, é apenas um exercício matemático para provar que a atração eletrostática que o retículo cristalino exerce sobre cada cátion, é máxima quando os cátions estão na localização original da cela unitária. Apesar de existirem 14 possibilidades de organizar átomos no espaço tridimensional, a natureza selecionou apenas 3 para a maior parte dos metais - por quê? A natureza escolheu a estrutura cristalina, de forma a: - Maximizar a coesão do retículo cristalino, - através da maximização do volume ocupado nas celas unitárias. Consideremos uma cela unitária de Cobre formada por 4 íons positivos e uma carga de prova com o sinal e a magnitude de 4 elétrons, localizada no seu centro. No centro da cela unitária há 4 elétrons liberados por 4 cátions. Cada cátion está submetido à atração eletrostática da carga de prova e à repulsão dos demais cátions. Pela lei de Coulomb, calculamos a atração e a repulsão sobre cada cátion e obtemos as respectivas forças resultantes, que são atrativas. "Afastando" os cátions, a força resultante atrativa sobre cada cátion diminui. "Aproximando" os cátions acontece o oposto: a força resultante atrativa sobre cada cátion aumenta. Continuando a "aproximação", as forces resultants atrativas diminuem, até se tornarem nulas. "Aproximando" ainda mais os cátions, as forças de repulsão superam as de atração e as forças resultantes tornam-se repulsivas. No ponto de equilíbrio, que corresponde à posição dos cátions na cela unitária, as forças resultantes atrativas são máximas. No ponto de equilíbrio, se o metal fosse formado por átomos neutros, eles se tangenciariam. No ponto de equilíbrio também se verifica a maior ocupação do volume da cela unitária. Os átomos ocupam 74% do volume da cela unitária Cúbica de Face-Centrada (FCC- Face-Centered Cubic) Os átomos ocupam 68% do volume da cela unitária da cela unitária Cúbica de Corpo-Centrado (BCC- Body-Centered Cubic). Para facilitar o cálculo do volume ocupado, vamos usar apenas uma das 3 celas unitárias do Empacotamento Hexagonal Denso. A área da base da cela unitária é igual a 2 vezes a área da base do triângulo equilátero. A altura da cela unitária é igual a 2 vezes a altura do tetraedro com arestas 2r. Os átomos ocupam 74% do volume da cela unitária do Empacotamento Hexagonal Denso (HCP- Hexagonal Closest Packing).
Compartilhar